摘要
背景
脑淀粉样血管病(Cerebral amyloid angiopopathy, CAA)发生在80%的阿尔茨海默病(Alzheimer 's disease, AD)患者中,主要由脑血管壁上Aβ的异常沉积引起。采用全面准确的定量蛋白质组学方法研究CAA的脑血管分子机制。
方法
针对CAA特异性分子机制,分别对伴有严重皮质Aβ血管沉积(ADNC +/CAA +)的AD神经病变(ADNC)患者和无Aβ血管沉积(ADNC +/CAA−)的ADNC患者制备了福尔马林固定石蜡包埋(FFPE)切片。所谓的,AD)。使用激光显微解剖(LMD)从FFPE切片中分离大脑皮质血管,通过压力循环技术(PCT)进行处理,并应用于SWATH (sequential window acquisition of all theoretical fragment ion spectra)蛋白质组学。
结果
ADNC +/CAA +/H供体(ADNC +/CAA +供体毛细血管中Aβ含量高)中17种蛋白的表达水平与ADNC +/CAA -和ADNC - /CAA -供体有显著差异。此外,我们鉴定出56种蛋白质在ADNC +/CAA +和ADNC - /CAA -供体之间的平均表达水平差异超过1.5倍,并且在11个供体(6个ADNC +/CAA +和5个ADNC - /CAA -)中与a β或胶原α -2(VI)链(COL6A2) (CAA标记物)水平显著相关。56个蛋白中超过70%的蛋白表达出现ADNC +/CAA +特异性变化。与脑实质对比分析表明,56种蛋白90%以上为血管特异性病变。一项基于文献的通路分析显示,42种蛋白与纤维化、氧化应激和细胞凋亡有关。这包括热休克蛋白HSP 90- α、CD44抗原和碳酸酐酶1的表达增加,这些蛋白被潜在的抗CAA药物抑制。
结论
结合基于lmd的FFPE切片血管分离、pct辅助样品处理和SWATH分析(FFPE- lmd - pct -SWATH方法),首次揭示了ADNC +/CAA + (CAA患者)血管中参与纤维化、ROS产生和细胞死亡的许多蛋白的表达变化。本文所报道的研究结果将有助于更好地了解CAA的病理,并促进CAA药物和生物标志物的发现和开发。
背景
脑淀粉样血管病(Cerebral amyloid angiopopathy, CAA)发生在80%的阿尔茨海默病(Alzheimer 's disease, AD)患者中,主要由脑血管壁上Aβ的异常沉积引起。这种沉积最终导致血管内皮细胞纤维化和凋亡,从而导致中风和脑出血等致命疾病[1,2]。然而,这种疾病仍然没有有效的治疗方法,鉴于其广泛性,寻找CAA的药物靶点是很重要的。因此,阐明CAA患者脑血管系统的病理分子机制是很重要的。
与传统的散弹枪蛋白质组学相比,SWATH方法是一种高度精确和可重复性高的综合蛋白质组学方法,对于定量确定病理状态下蛋白质的表达水平非常有用[3.]。由于Aβ在CAA患者的皮质血管中积累,有必要选择性地采集血管作为样本。激光显微解剖(LMD)血管在福尔马林固定,石蜡包埋(FFPE)切片已被证明是有效的,但从FFPE切片获得的蛋白质组学数据不像那些从未固定的新鲜组织,由于亚甲基交联在FFPE切片。正因为如此,使用FFPE切片收集蛋白质组学数据很难准确地阐明这种情况的病理分子机制。然而,我们最近使用压力循环技术(PCT)在高温高压(比大气压高3000倍)下去除交联样品,以完全消除交联[3.]。我们将使用FFPE切片结合pct辅助样品处理的SWATH蛋白质组学称为“FFPE- pct -SWATH方法”。通过我们建立的FFPE-PCT-SWATH方法,我们能够获得清晰反映未固定新鲜组织分子机制的蛋白质组学数据[3.]。
在这项研究中,我们使用LMD从FFPE切片中分离血管,进行pct辅助样品处理和SWATH分析,以阐明CAA的分子机制。为了阐明CAA病理特异性的分子机制,我们不仅制备了伴有严重皮层Aβ血管沉积的AD神经病变(ADNC)患者(ADNC +/CAA +组)的FFPE切片,还制备了伴有严重皮层Aβ血管沉积的AD神经病变(ADNC)患者(ADNC +/CAA -组)和无血管沉积的AD神经病变(ADNC +/CAA -组)的FFPE切片。
材料与方法
人脑FFPE切片
获得FFPE切片的枕叶神经病理信息汇总于表中1.FFPE切片由三原纪念医院脑库提供。神经病理学评估基于国家阿尔茨海默病协调中心的“NIA阿尔茨海默病研究中心计划(v11)”(https://naccdata.org/data-collection/forms-documentation/np-11).采用美国国家衰老研究所-阿尔茨海默病协会(NIA-AA)指南(2012)来确定AD的病理改变水平[4]基于先前描述的神经病理分析[5]。通过Aβ血管沉积的免疫组织化学分析确定AD脑是否包含CAA病理(图2)。1).当AD病理改变水平为“中高”并伴有中重度CAA时,将患者分为ADNC +/CAA +组。在FFPE切片中观察到该组在所有皮质血管中均有Aβ沉积。无CAA的“中度”病理改变的病例被分配到ADNC +/CAA -组。没有Aβ免疫反应性沉积的病例被分配到ADNC - /CAA -组。Aβ和COL6A2的表达水平见表1为本研究中SWATH分析获得的实验结果(不是ELISA),不用于区分ADNC +/CAA +、ADNC +/CAA -和ADNC - /CAA -组。通过Aβ40和Aβ42共享的色氨酸“LVFFAEDVGSNK”的峰面积来定量Aβ40和Aβ42的总水平(不单独)。枕叶CAA病变最明显[6],很少有神经原纤维缠结,没有突触核蛋白沉积。由于这个原因,枕叶被使用,因为它比其他大脑区域更适合于阐明caa衍生的病理分子机制。本研究的方案由三原纪念医院伦理委员会(协议代码095-06,于2019年1月16日批准)和东北大学药学研究生院(协议代码18-03,于2018年12月20日批准)批准。所有参与研究的受试者都获得了书面知情同意。
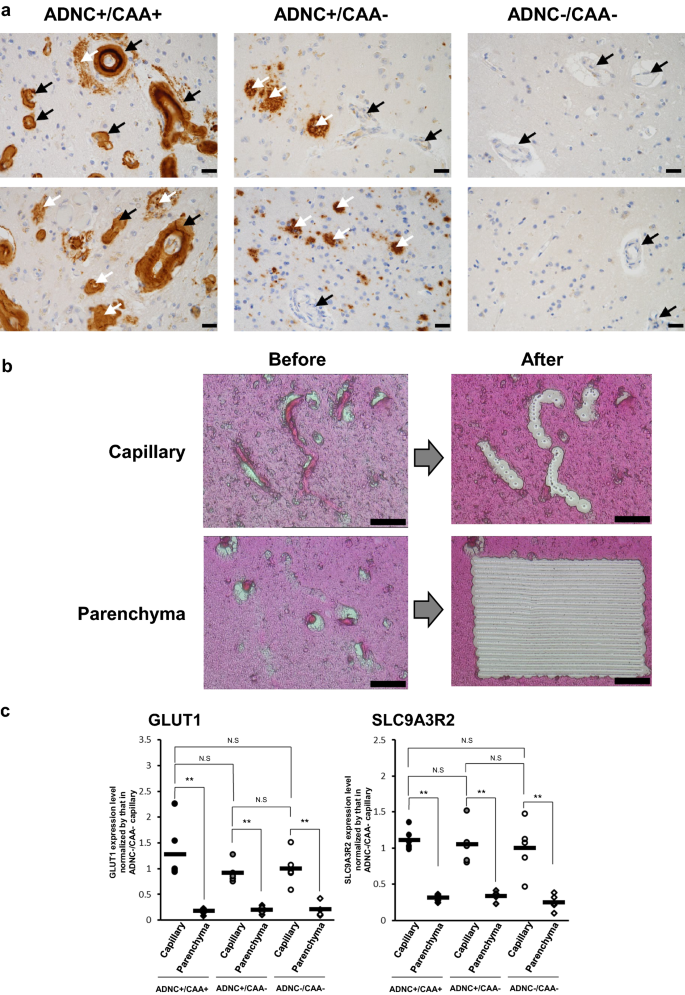
LMD分离脑皮质毛细血管和脑实质及分离毛细血管纯度的验证。一个使用ADNC +/CAA +、ADNC +/CAA -和ADNC - /CAA -组的FFPE切片进行Aβ免疫染色,如前所述[5]。每组显示两张不同地区的照片。黑色箭头表示枕叶皮层的脑血管。白色箭头表示皮层实质(血管除外)内的Aβ沉积。比例尺,20µm。ADNC +/CAA +切片显示皮质区所有血管均被Aβ覆盖。对每组相邻切片进行蛋白质组学分析(伊红染色)。bLMD前后的伊红染色照片。比例尺,50µm。伊红染色可以在FFPE切片上识别出脑血管和皮层区域。如图所示,用LMD分离皮层血管(除大血管外)和薄壁组织,直至总解剖面积达到15mm2(× 20 μm厚度= 0.3 mm3.)。c两种内皮细胞标志物在收集的毛细血管和薄壁组织中的相对蛋白表达水平。每个蛋白的表达水平通过ADNC - /CAA -毛细血管中蛋白表达水平的平均值归一化,如“材料与方法”一节。黑色图,ADNC +/CAA +;灰色图,ADNC +/CAA−;白色图,ADNC−/CAA−。圈,毛细管样品;钻石,实质样本。**经bh校正p < 0.01,两组间差异有统计学意义。NS差异无统计学意义(经bh校正p > 0.01)
制备用于蛋白质组学分析的FFPE切片
从FFPE块中获得切片(厚度为20 μm),切片安装在定向激光显微解剖载玻片上(AMR Inc., Cat. 50001-024, Tokyo, Japan)。载玻片的FFPE切片分别在二甲苯(3 × 5 min)、无水乙醇(2 × 1 min)、95% (v/v)乙醇(2 × 1 min)、70%乙醇(2 × 1 min)和milliq水(1 min)中孵育。去胶切片在milliq水中孵育(5分钟),用伊红染色(1分钟),然后在自来水中洗涤(15分钟)。
激光显微解剖(LMD)
上面的伊红染色显示了脑血管。为了避免在免疫染色过程中蛋白分子在解交联后被降解的风险,我们没有对Aβ进行免疫染色,而是进行了伊红染色,这样可以在LMD过程中保持固定。对于ADNC +/CAA +组,我们使用FFPE切片,其中皮质区域的所有血管都被Aβ覆盖,使用邻近切片进行免疫组织化学分析。
LMD使用Leica LMD6000系统(Leica Microsystems GmbH, Wetzlar, Germany)进行。CAA中的Aβ沉积仅在皮层中,而不在白质中。伊红染色可以将皮层与白质区分开来。为了获得用于蛋白质组学分析的皮质薄壁组织,随机解剖伊红染色切片的皮质区域,直到总解剖面积达到15mm2(× 20 μm厚度= 0.3 mm3.)(图。1).为了获得用于蛋白质组学分析的皮质血管,对伊红染色切片中皮质区域的血管(大血管除外)进行随机解剖,直至总解剖面积达到15mm2(× 20 μm厚度= 0.3 mm3.)(图。1).
在LMD系统中,将FFPE切片的解剖样本直接收集在含有20µl相转移表面活性剂(PTS)缓冲液的管(0.5 ml PCR tube with Flat cap, Thin-Wall, Non-Sterile, MaxyClear)的帽中。将收集到的20µl FFPE组织悬浮液转移到PCT Micro Tube中,将20µl PTS缓冲液加入杯中,将该溶液转移到PCT Micro Tube中。重复此过程两次,共将60µl FFPE组织悬浮液转移到PCT Micro Tube中,然后用PCT Micro Cap(50µl大小)覆盖PCT Micro Cap。
从FFPE中提取蛋白质,用PCT处理制备蛋白质样品
所有样品在块培养箱中95°C孵育60分钟(Eppendorf, Hamburg, Germany;与混合在1000转/分)。之后,FFPE样品在barocycle (NEP 2320 Enhanced;Pressure BioSciences, South Easton, MA)分两步进行:首先,在45000 psi压力下进行60个95秒的循环,在95°C的大气压下进行5秒,其次,在45000 psi压力下进行50个20秒的循环,在95°C的大气压下进行15秒。
经PCT处理的FFPE样品的蛋白质消化
蛋白质提取后尽快进行蛋白质消化。在15,000 rpm和室温下离心3分钟后,将40 μl等分的上清液转移到装有PCT Micro cap(尺寸为150 μl)的新型PCT Micro Tubes中(Pressure BioSciences, South Easton, MA)。样品用10 mM(±)-二硫苏糖醇(DTT) (Wako Pure Chemical Industries,大阪,日本)在25°C下处理30分钟,然后用40 mM碘乙酰胺(IAA) (Wako Pure Chemical Industries,大阪,日本)在25°C下黑暗烷基化。在加入蛋白酶Max表面活性剂(Promega, Madison, WI)和Lys-C (Wako Pure Chemical Industries, Osaka, Japan),末浓度为0.04%,酶/底物比为1:20之前,用50 mM碳酸氢铵调节缓冲体积至139 μl对样品进行稀释。在37°C的barcycler中进行pct辅助的Lys-C消化,在45,000 psi下进行60次循环,50 s,在大气压下进行10 s。胰蛋白酶(Promega, Madison, WI)以酶/底物比例1:20加入蛋白酶Max表面活性剂。在37°C的Barocycler中进行pct辅助胰蛋白酶消化,在45,000 psi下进行90次循环,50秒,在大气压下进行10秒。酶解后,用乙酸乙酯液-液萃取法去除SDC和SLS (PTS)。水相在真空下干燥,在- 80°C保存,直到脱盐。肽样品溶解于0.1%三氟乙酸/水中,用自包装的SDB-XD尖(3m, Maplewood, MN)脱盐,洗脱后的肽溶液再次真空干燥。 Peptides samples were dissolved in 0.1% formic acid/2% acetonitrile/98% water, and their concentration was adjusted to 0.5 μg/μl based on the BCA assay (for parenchymal sample, but was not adjusted for vessel sample). The recovery from a 0.3 mm3.FFPE切片肽数为8.22±3.29µg (mean±SD)。
利用纳米olc - tripletof5600系统进行SWATH测量
SWATH-MS测量和分析按前面所述进行[3.]。1µg肽被应用于纳米lc ultra (Eksigent Technologies, Dublin, CA, USA),结合电喷雾电离三重TOF 5600质谱仪(SCIEX, Framingham, MA, USA)。
基于swath的定量蛋白质组学数据分析
光谱比对和SWATH色谱的数据提取(上传到肽图谱网站,识别码为PASS01719)使用Peakview (SCIEX)的SWATH处理微应用程序使用内部光谱库(上传到肽图谱网站,识别码为PASS01719)进行,如前所述[3.,7]。根据先前描述的程序[7],根据数据选择标准和基于氨基酸序列的多肽选择标准剔除不可靠的峰和肽,将不同过渡之间的信号强度差异归一化后,计算多肽水平的峰面积为过渡水平峰面积的平均值。此程序的详情已于先前报道[7]。单个蛋白质的峰面积计算为肽水平峰面积的平均值。对于每种蛋白,最后将单个供体中蛋白的峰面积除以5个ADNC - /CAA -供体毛细管样品中蛋白峰面积的平均值,得到蛋白的相对表达水平(附加文件)2:表1)。
统计分析
所有统计分析均在零假设下进行,假设比较组的平均值相等。两组间比较采用非配对双尾t检验,多组比较采用Benjamini-Hochberg (BH)校正校正p值。相关分析采用Excel 2010版统计软件计算Spearman等级相关系数和p值。如果p值小于0.05,则认为差异具有统计学意义,拒绝原假设。没有进行正式的功率计算来估计所需的样本量。本研究未采用随机化或盲法。
结果
分离毛细管的纯度验证
为了证实LMD分离的皮质血管的纯度,我们比较了内皮细胞标记蛋白葡萄糖转运蛋白1 (GLUT1)和Na的表达水平+/小时+交换调节辅助因子NHE-RF2 (SLC9A3R2),据报道,该因子在人类蛋白质图谱中在脑血管中特异性表达(https://www.proteinatlas.org/),在ADNC +/CAA +、ADNC +/CAA -和ADNC - /CAA -组的FFPE切片中收集的毛细血管和薄壁组织中。3个供体组收集的毛细血管中3种蛋白的表达水平均无显著差异(p > 0.01)(图2)。1).两种蛋白在收集的毛细血管中的表达水平均显著高于收集的薄壁组织(p < 0.01)。1).结果表明,ADNC +/CAA +组、ADNC +/CAA -组和ADNC - /CAA -组毛细血管内皮细胞富集,内皮细胞纯度相同。
收集的毛细血管中ADNC +/CAA +/H、ADNC +/CAA +/L、ADNC +/CAA−和ADNC - /CAA−组蛋白表达水平的组间差异
对收集到的毛细血管和薄壁组织进行SWATH分析,结果显示有1255个蛋白被量化(附加文件)2:表1)。由于蛋白表达水平的个体差异较大,对于ADNC +/CAA +组,将毛细血管中Aβ含量较高的3个供者(供者1、2、3)归类为“ADNC +/CAA +/H”,将其他3个供者(供者4、5、6)归类为“ADNC +/CAA +/L”。为了鉴定与CAA病理特异性相关的蛋白质,提取满足以下(1)和(2)标准的蛋白质;(1) ADNC +/CAA +/H组与ADNC +/CAA -组之间,(2)ADNC +/CAA +/H组与ADNC - /CAA -组之间,所收集的毛细血管蛋白表达水平存在显著差异(经bh调整p < 0.05)。共提取蛋白17个,其中纤维化相关蛋白1个,ROS相关蛋白2个,抗氧化相关蛋白2个,Akt相关蛋白2个,caspase相关蛋白4个,其他蛋白6个(表2)2).由于蛋白表达水平存在较大的个体差异,因此通过以下相关分析进一步筛选caa相关蛋白。
蛋白表达水平与Aβ或胶原α -2(VI)链(COL6A2)的相关性
假设血管中存在的a β的数量是疾病严重程度的指标,ADNC +/CAA +组的6例患者的严重程度差异为120倍,表明个体差异很大(表1)1).我们假设与疾病相关的蛋白质会随着疾病的严重程度而改变。COL6A2是本研究中被量化的一种蛋白质,据报道,在ADNC +/CAA +患者的血管中积累,Aβ也是如此[8]。在本研究中,将Aβ和COL6A2作为疾病严重程度的指标,并利用这些分子与其他蛋白之间的相关性来缩小可能与CAA病理相关的候选蛋白。仅对6个ADNC +/CAA +样品进行Spearman等级相关分析并不能使我们确定有希望的蛋白质,因为该分析未能成功排除表达水平与ADNC - /CAA -组没有差异的蛋白质。因此,我们使用以下两种选择提取候选蛋白:(1)收集到的6个ADNC +/CAA +和5个ADNC - /CAA -供者的毛细血管平均表达水平差异超过1.5倍的蛋白质;(2)根据Spearman等级相关分析,11个供者(6个ADNC +/CAA +和5个ADNC - /CAA -供者)中与a β或COL6A2显著(p < 0.05)相关的蛋白质。有43种蛋白符合这两个标准,并与Aβ显著相关(表2)3.)和46个与COL6A2显著相关的蛋白(附加文件2表2)。为了确定这些蛋白的表达变化是否只发生在ADNC +/CAA +患者的毛细血管中(而不发生在ADNC +/CAA -患者的毛细血管中,也不发生在ADNC +/CAA +和ADNC +/CAA -患者的实质中),我们使用ADNC +/CAA -患者的毛细血管和实质的数据对这些蛋白进行了Spearman相关分析。在毛细血管中,43种蛋白中只有5种与Aβ显著相关(表2)3.), 46个蛋白中只有8个含有COL6A2(附加文件)2表S2)使用10个供者(5个ADNC +/CAA -和5个ADNC - /CAA -供者)进行Spearman相关分析。在薄壁组织中,43种蛋白中只有1种与Aβ显著相关(表2)3.46个蛋白中只有2个与COL6A2显著相关(附加文件)211例供体(6例ADNC +/CAA +和5例ADNC - /CAA -供体)的Spearman相关分析见表S2。在使用来自10个供体(5个ADNC +/CAA -和5个ADNC - /CAA -供体)的实质进行的Spearman相关分析中,没有蛋白(在43个蛋白中)与Aβ显著相关(表2)3.), 46个蛋白中只有8个与COL6A2显著相关(附加文件2表2)。
细胞外基质成分蛋白
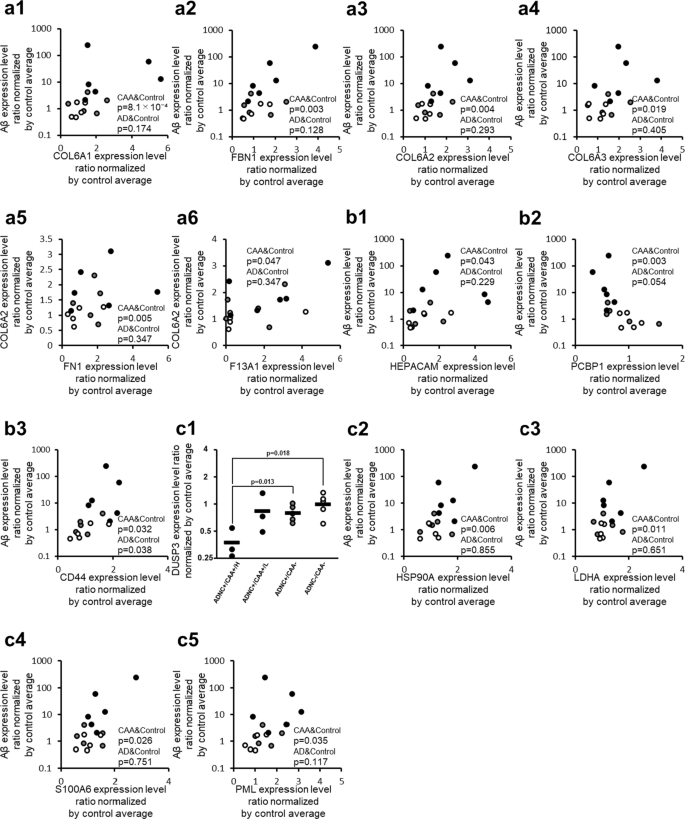
根据11个ADNC +/CAA +和ADNC - /CAA -供体的Spearman等级相关系数,在构成ECM并有助于其稳定的蛋白中,与a β呈显著(p < 0.05)正相关的蛋白有胶原α -1(VI)链(COL6A1;p = 8.07 × 104)、纤颤蛋白1 (FBN1;p = 3.11 × 103), COL6A2 (p = 4.47 × 10)3胶原α -3(VI)链(COL6A3;p = 1.86 × 102)在毛细管样品中(图2)。2和表3.).无蛋白呈负相关。同样,在11例ADNC +/CAA +和ADNC - /CAA -供者中,与COL6A2呈显著正相关(p < 0.05)的蛋白为COL6A3 (p = 8.40 × 10)8), COL6A1 (p = 3.30 × 104),纤维连接蛋白(FN1;p = 5.30 × 103), FBN1 (p = 9.76 × 10)3),凝血因子XIII A链(F13A1;p = 4.67 × 102),毛细血管样品中无蛋白呈负相关(图2)。2和附加文件2表2)。在毛细管样品中使用10个ADNC +/CAA -和ADNC - /CAA -供体进行Spearman等级相关分析时,这些蛋白均未显示出与a β的显著相关性(图2)。2).图6所示的6种ecm相关蛋白。2,所采集的毛细血管组间比较图也见附加文件1:图S2,但ADNC +/CAA +/H组和ADNC +/CAA−组间无显著差异(经bh校正p > 0.05)。
收集的毛细血管中纤维化相关分子蛋白表达水平的caa特异性变化。表中列出的纤维化相关分子2,该图优先展示了它们组间比较的曲线图。表中未列出的纤维化相关分子2但列于表3.或附加文件2:表S2,若该蛋白与a β均表现出显著相关性,则该图为与a β的相关图(表2)3.)和COL6A2(附加文件2表2)。一个ECM-related蛋白质,b细胞- ecm黏附相关蛋白;cTGF-β信号相关蛋白。个体供者的蛋白质表达水平数据(按ADNC - /CAA -毛细血管中蛋白质表达水平的平均值归一化)材料与方法”部分),取自“附加文件”2表S1。黑图表示ADNC +/CAA + (CAA);灰色图,ADNC +/CAA−(AD);白色图,ADNC−/CAA−(Control)。对于ADNC +/CAA +组,将毛细血管中Aβ含量较高的3个供者(供者1、2、3)归类为“ADNC +/CAA +/H”,其余3个供者(供者4、5、6)归类为“ADNC +/CAA +/L”。p值取自表格2,3.或附加文件2表S2。在相关图中,“CAA& control”和“AD&Control”的p值分别代表11个供体(ADNC +/CAA +和ADNC - /CAA -)和10个供体(ADNC +/CAA -和ADNC - /CAA -)的Spearman等级相关值
粘附分子
在参与细胞与ECM黏附的蛋白中,根据11个ADNC +/CAA +和ADNC - /CAA -供体的Spearman等级相关系数,与a β呈显著正相关的蛋白有CD44抗原(CD44;p = 3.20 × 10−2)和肝细胞粘附分子(HEPACAM;p = 4.26 × 10−2)在毛细管样品中(图2)。2和表3.).Poly(rC)-binding protein 1 (PCBP1;p = 2.56 × 10−3).对于这三种分子,相关性的p值低于使用10个ADNC +/CAA -和ADNC - /CAA -供体的分子(图2)。2).同样,在11例ADNC +/CAA +和ADNC - /CAA -供体中,与COL6A2呈显著正相关(p < 0.05)的蛋白是CD44 (p = 1.86 × 10)−2).(p = 8.43 × 10−3)在毛细管样品中呈负相关(附加文件2表2)。对于图中所示的3种粘附分子。2,所采集的毛细血管组间比较图也见附加文件1:图S2,但ADNC +/CAA +/H组和ADNC +/CAA−组间无显著差异(经bh校正p > 0.05)。
Fibrosis-associated蛋白质
ADNC +/CAA +/H组双特异性蛋白磷酸酶3 (DUSP3)蛋白表达水平显著低于ADNC +/CAA -和ADNC - /CAA -组(经bh调整p < 0.05)。2和表2).11例ADNC +/CAA +和ADNC - /CAA -供体与纤维化相关的蛋白中,与a β呈显著(p < 0.05)正相关的蛋白有热休克蛋白hsp90 - α (HSP90A;p = 6.23 × 10−3), l -乳酸脱氢酶A链(LDHA;p = 1.12 × 10−2),蛋白质S100-A6 (S100A6;p = 2.60 × 10−2蛋白PML (PML;p = 3.53 × 10−2)在毛细管样品中(图2)。2和表3.).DUSP3呈负相关(p = 4.47 × 10)−3).在毛细管样品中使用10个ADNC +/CAA -和ADNC - /CAA -供体进行Spearman等级相关分析时,这些蛋白均未显示出与a β的显著相关性(图2)。2).同样,在11例ADNC +/CAA +和ADNC - /CAA -供者中,与COL6A2呈显著正相关(p < 0.05)的蛋白为S100A6 (p = 4.55 × 10)−4PML (p = 8.45 × 10)−3)、LDHA (p = 3.53 × 10)−2HSP90A (p = 3.53 × 10)−2).DUSP3 (p = 3.20 × 10−2)在毛细管样品中呈负相关(附加文件2表2)。图中4个TGF-β信号相关蛋白的相关图。2,所采集的毛细血管组间比较图也见附加文件1:图S2,但ADNC +/CAA +/H组与ADNC +/CAA-组间差异无统计学意义(经bh校正p > 0.05)。
氧化应激相关蛋白
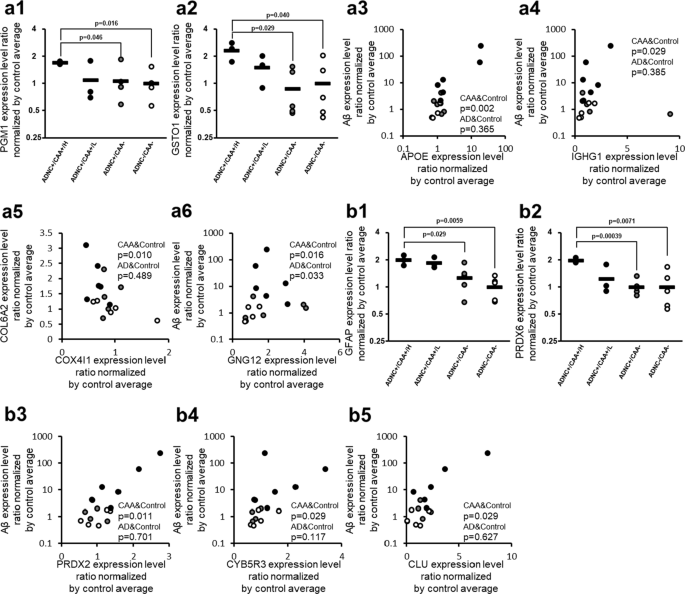
ADNC +/CAA +/H供体中磷酸葡萄糖糖糖化酶-1 (PGM1)和谷胱甘肽s -转移酶-1 (GSTO1)的蛋白表达水平显著高于ADNC +/CAA -和ADNC - /CAA -供体(经bh调整p < 0.05)(图2)。3.和表2).在参与氧化应激的蛋白中,根据11 ADNC +/CAA +和ADNC - /CAA -供体的Spearman等级相关系数,与a β呈显著(p < 0.05)正相关的蛋白有载脂蛋白E (APOE);p = 1.68 × 10−3),鸟嘌呤核苷酸结合蛋白G(I)/G(S)/G(O)亚基γ -12 (GNG12);p = 1.65 × 10−2), GSTO1 (p = 2.33 × 10)−2)和免疫球蛋白重常数γ 1 (IGHG1;p = 2.89 × 10−2)在毛细管样品中(图2)。3.和表3.).只有GNG12 (p = 3.30 × 10)−2)在使用10个ADNC +/CAA -和ADNC - /CAA -供体的毛细管样品的Spearman等级相关分析中显示出与a β显著正相关(图2)。3.),但GNG12的p值大于11例ADNC +/CAA +和ADNC - /CAA -供体的p值。同样,在11例ADNC +/CAA +和ADNC - /CAA -供体中,与COL6A2呈显著正相关(p < 0.05)的蛋白为APOE (p = 3.30 × 10)−4), GSTO1 (p = 4.47 × 10)−3)、GNG12 (p = 4.67 × 10)−2).线粒体细胞色素c氧化酶亚基4亚型1 (COX4I1);p = 9.76 × 10−3)在毛细管样品中呈负相关(图2)。3.和附加文件2表2)。在毛细管样品中使用10个ADNC +/CAA -和ADNC - /CAA -供体进行Spearman等级相关分析,这些蛋白均未显示出与COL6A2的显著相关性(附加文件)2表2)。图4所示4种ros相关蛋白的相关图。3.,所采集的毛细血管组间比较图也见附加文件1:图S3,但ADNC +/CAA +/H组和ADNC +/CAA−组间无显著差异(经bh校正p > 0.05)。
收集的毛细血管中氧化应激相关分子蛋白表达水平的caa特异性变化。表中列出的氧化应激相关蛋白2,显示其组间比较的图表优先呈现在该图中。表中未列出的氧化应激相关蛋白2但列于表3.或附加文件2:表S2,若该蛋白与a β均表现出显著相关性,则该图为与a β的相关图(表2)3.)和COL6A2(附加文件2表2)。一个ros相关蛋白,以及bAntioxidant-related蛋白质。个体供者的蛋白质表达水平数据(按ADNC - /CAA -毛细血管中蛋白质表达水平的平均值归一化)材料与方法”部分),取自“附加文件”2表S1。黑图表示ADNC +/CAA + (CAA);灰色图,ADNC +/CAA−(AD);白色图,ADNC−/CAA−(Control)。对于ADNC +/CAA +组,将毛细血管中Aβ含量较高的3个供者(供者1、2、3)归类为“ADNC +/CAA +/H”,其余3个供者(供者4、5、6)归类为“ADNC +/CAA +/L”。p值取自表格2,3.或附加文件2表S2。在相关图中,“CAA& control”和“AD&Control”的p值分别代表11个供体(ADNC +/CAA +和ADNC - /CAA -)和10个供体(ADNC +/CAA -和ADNC - /CAA -)的Spearman等级相关值
抗氧化蛋白
ADNC +/CAA +/H供体的胶质纤维酸性蛋白(GFAP)和过氧化物还蛋白-6 (PRDX6)的蛋白表达水平显著高于ADNC +/CAA -和ADNC - /CAA -供体(ph调整后p < 0.05)。3.和表2).在抗氧化蛋白中,根据11个ADNC +/CAA +和ADNC - /CAA -供体的Spearman等级相关系数,与a β呈显著(p < 0.05)正相关的蛋白为GFAP (p = 6.12 × 10)−4)、过氧化物还原素-2 (PRDX2;p = 1.12 × 10−2), nadh -细胞色素b5还原酶3 (CYB5R3;p = 2.89 × 10−2)、Clusterin (CLU;p = 2.89 × 10−2)、PRDX6 (p = 3.88 × 10)−2)在毛细管样品中(图2)。3.和表3.).同样,在11个ADNC +/CAA +和ADNC - /CAA -供体中,与COL6A2呈显著正相关(p < 0.05)的蛋白是CLU (p = 3.75 × 10)−3)、GFAP (p = 1.12 × 10)−2), PRDX6 (p = 1.12 × 10)−2), CYB5R3 (p = 1.65 × 10)−2)(附加文件2表2)。在毛细管样品中使用10个ADNC +/CAA -和ADNC - /CAA -供体进行Spearman等级相关分析时,这些蛋白均未显示出与a β或COL6A2的显著相关性。3.、表3.,以及附加文件2表2)。图3所示的3种抗氧化剂相关蛋白的相关性图。3.,所采集的毛细血管组间比较图也见附加文件1:图S3,但ADNC +/CAA +/H组和ADNC +/CAA−组间无显著差异(经bh校正p > 0.05)。
AKT信号蛋白
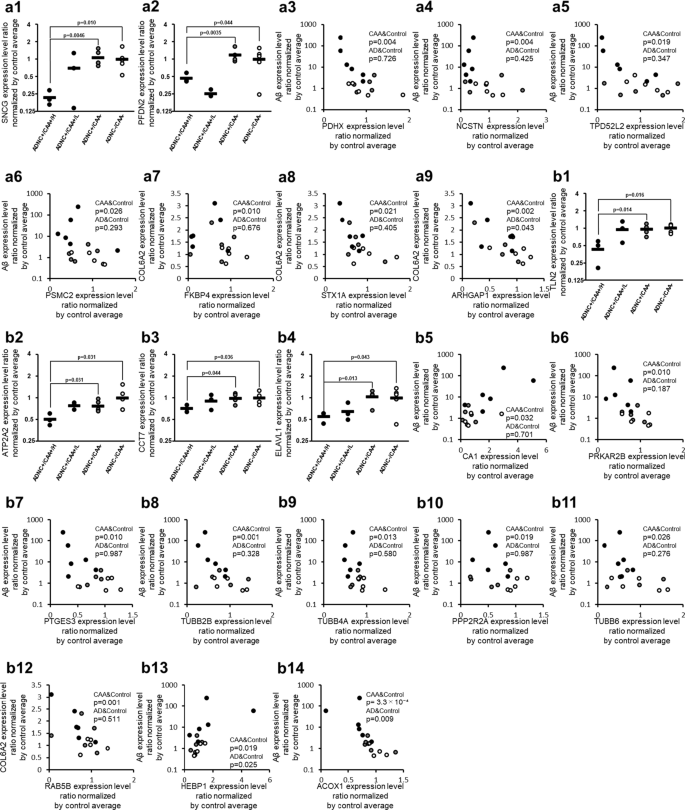
在ADNC +/CAA +/H供体中,γ -突触核蛋白(SNCG)和预折叠蛋白亚基2 (PFDN2)的蛋白表达水平显著低于ADNC +/CAA -和ADNC - /CAA -供体(bh调整p < 0.05)(图2)。4和表2).在参与AKT信号传导的蛋白中,对毛细管样品中11个ADNC +/CAA +和ADNC - /CAA -供体进行Spearman秩相关分析,未发现与a β或COL6A2显著正相关的蛋白(表2)3.和附加文件2表2)。与a β呈显著负相关的蛋白有线粒体丙酮酸脱氢酶蛋白X组分(PDHX;p = 3.75 × 10−3)、尼卡斯特林(NCSTN;p = 4.47 × 10−3),肿瘤蛋白D54 (TPD52L2;p = 1.86 × 10−2)和26S蛋白酶体调控亚基7 (PSMC2;p = 2.60 × 10−2)(图。4和表3.).与COL6A2呈显著负相关的蛋白为NCSTN (p = 1.05 × 10)−3), Rho gtpase激活蛋白1 (ARHGAP1;p = 2.08 × 10−3),肽基脯氨酸顺式反式异构酶FKBP4 (FKBP4;p = 9.76 × 10−3), Syntaxin-1A (STX1A;p = 2.08 × 10−2PDHX (p = 2.08 × 10)−2)在毛细管样品中(图2)。4和附加文件2表2)。只有ARHGAP1 (p = 4.25 × 10)−2)在Spearman等级相关分析中显示COL6A2与10个ADNC +/CAA -和ADNC - /CAA -供体的毛细管样品呈显著负相关(图2)。4),但ARHGAP1的p值大于11例ADNC +/CAA +和ADNC - /CAA -供者。图中7个AKT信号相关蛋白的相关图。4,所采集的毛细血管组间比较图也见附加文件1:图S4。与ADNC +/CAA +/H组相比,ADNC +/CAA +/H组PDHX和TPD52L2蛋白的表达水平显著降低,而ADNC +/CAA +/H组和ADNC +/CAA -组之间其他5种蛋白的表达水平无显著差异(经bh校正p > 0.05)。
收集的毛细血管中凋亡相关分子蛋白表达水平的caa特异性变化。凋亡相关蛋白见表12,显示其组间比较的图表优先呈现在该图中。表中未列出的凋亡相关蛋白2但列于表3.或附加文件2:表S2,若该蛋白与a β均表现出显著相关性,则该图为与a β的相关图(表2)3.)和COL6A2(附加文件2表2)。一个AKT信号相关蛋白,以及b半胱天冬酶信号相关蛋白。个体供者的蛋白质表达水平数据(按ADNC - /CAA -毛细血管中蛋白质表达水平的平均值归一化)材料与方法”部分),取自“附加文件”2表S1。黑图表示ADNC +/CAA + (CAA);灰色图,ADNC +/CAA−(AD);白色图,ADNC−/CAA−(Control)。对于ADNC +/CAA +组,将毛细血管中Aβ含量较高的3个供者(供者1、2、3)归类为“ADNC +/CAA +/H”,其余3个供者(供者4、5、6)归类为“ADNC +/CAA +/L”。p值取自表格2,3.或附加文件2表S2。在相关图中,“CAA& control”和“AD&Control”的p值分别代表11个供体(ADNC +/CAA +和ADNC - /CAA -)和10个供体(ADNC +/CAA -和ADNC - /CAA -)的Spearman等级相关值
Caspase信号蛋白
ADNC +/CAA +/H供体中Talin-2 (TLN2)、肌浆/内质网钙atp酶2 (ATP2A2)、t复合物蛋白1亚基(CCT7)和elav样蛋白1 (ELAVL1)的蛋白表达水平显著低于ADNC +/CAA -和ADNC - /CAA -供体(H调整p < 0.05)。4和表2).在参与caspase信号传导的蛋白中,根据11个ADNC +/CAA +和ADNC - /CAA -供体的Spearman等级相关系数,与a β呈显著(p < 0.05)正相关的蛋白有血红素结合蛋白1 (HEBP1;p = 1.86 × 10−2)和碳酸酐酶1 (CA1;p = 3.20 × 10−2)在毛细管样品中(图2)。4和表3.).与a β呈显著负相关的蛋白有:过氧化物酶体酰基辅酶a氧化酶1 (ACOX1;p = 3.30 × 10−4), ATP2A2 (p = 4.55 × 10)−4),微管蛋白β - 2b链(TUBB2B;p = 1.05 × 10−3),前列腺素E合成酶3 (PTGES3;p = 9.76 × 10−3), camp依赖性蛋白激酶ii型β调控亚基(PRKAR2B;p = 9.76 × 10−3),微管蛋白β - 4a链(TUBB4A;p = 1.28 × 10−2),丝氨酸/苏氨酸蛋白磷酸酶2A 55 kDa调节亚基B α亚型(PPP2R2A;p = 1.86 × 10−2)和微管蛋白β -6链(TUBB6;p = 2.60 × 10−2)(图。4和表3.).与COL6A2呈显著负相关的蛋白为TUBB4A (p = 2.21 × 10)−5), ras相关蛋白RAB5B (RAB5B;p = 1.33 × 10−3), ACOX1 (p = 8.45 × 10)−3), ATP2A2 (p = 1.12 × 10)−2), PPP2R2A (p = 1.86 × 10)−2PTGES3 (p = 2.33 × 10)−2), PRKAR2B (p = 3.53 × 10)−2), TUBB2B (p = 3.88 × 10)−2)(图。4和附加文件2表2)。Spearman等级相关分析使用10个ADNC +/CAA -和ADNC - /CAA -毛细血管样本供体,结果显示只有HEBP1与Aβ有显著相关性(p = 2.51 × 10)−2), ACOX1(与Aβ, p = 9.22 × 10)−3)和TUBB2B(含COL6A2, p = 3.88 × 10)−2)(图。4和附加文件2表2)。图中10个caspase信号相关蛋白的相关图。4,所采集的毛细血管组间比较图也见附加文件1:图S4,但ADNC +/CAA +/H组与ADNC +/CAA−组间无显著差异(经bh校正p > 0.05)。
其他蛋白质
ADNC +/CAA +/H组的缬氨酸- trna连接酶(VARS)、肝素- α -氨基葡萄糖n-乙酰转移酶(HGSNAT)、磷酸吡啶醇稳态蛋白(PLPBP)、可溶性无机热磷酸酶1 (PPA1)、突触囊泡糖蛋白2B (SV2B)和磷脂转移蛋白C2CD2L (C2CD2L)的蛋白表达水平与ADNC +/CAA -和ADNC - /CAA -组有显著差异(经H校正p < 0.05)(另附文件)1:图S1和表2).在与上述分子机制无关的蛋白质中,根据11个ADNC +/CAA +和ADNC - /CAA -供体的Spearman等级相关系数,与a β呈显著(p < 0.05)正相关的蛋白质是KN motif和锚蛋白重复结构域蛋白2 (KANK2;p = 5.30 × 10−3)(表13.和附加文件1:图S1)。与a β呈显著负相关的蛋白为VARS (p = 1.12 × 10)−5), α -肌动蛋白-2 (ACTN2;p = 2.08 × 10−3), Exocyst复合物6B (EXOC6B;p = 3.11 × 10−3),热休克蛋白105 kDa (HSPH1;p = 1.46 × 10−2), SV2B (p = 1.46 × 10)−2),线粒体电子转移黄蛋白亚基α (ETFA;p = 1.65 × 10−2)和苯丙氨酸- trna连接酶α亚基(FARSA;p = 1.86 × 10−2)(表3.和附加文件1:图S1)。与COL6A2呈显著正相关的蛋白有KANK2 (p = 4.47 × 10)−3)和蛋白酶体激活物复合体亚基1 (PSME1;p = 3.53 × 10−2HSPH1 (p = 3.97 × 10)−5), SV2B (p = 2.33 × 10)−4), EXOC6B (p = 6.12 × 10−4), VARS (p = 6.12 × 10)−4), ACTN2 (p = 8.45 × 10)−3), Noelin (OLFM1;p = 9.76 × 10−3), NADH脱氢酶1 α亚复合物亚基2 (NDUFA2;p = 1.65 × 10−2), NADH脱氢酶1 α亚复合物亚基8 (NDUFA8;p = 2.33 × 10−2), FARSA (p = 2.89 × 10)−2), ras相关蛋白raba - 3a (RAB3A;p = 3.88 × 10−2),以及聚腺苷酸结合蛋白4 (PABPC4;p = 4.26 × 10−2根据Spearman等级相关系数,在毛细管样品中使用11个ADNC +/CAA +和ADNC - /CAA -供体显示COL6A2显著负相关(附加文件)2:表S2和附加文件1:图S1)。其他12个未分类的蛋白在附加文件中以相关图显示1:图S1,采集的毛细血管组间比较图也见附加文件1:图S5,但ADNC +/CAA +/H组与ADNC +/CAA−组间无显著性差异(经bh校正p > 0.05)。
讨论
利用LMD从ADNC +/CAA +患者的FFPE切片中分离出a β积累的皮质血管后,我们将pct辅助的样品过程(允许完全解交联和胰蛋白酶消化)与SWATH方法(简称FFPE-LMD- pct -SWATH方法)全面准确的蛋白质定量相结合,揭示ADNC +/CAA +毛细血管的病理分子机制。ADNC +/CAA +/H组17种蛋白的表达水平与ADNC +/CAA -和ADNC - /CAA -组差异有统计学意义(经bh校正p < 0.05)2).
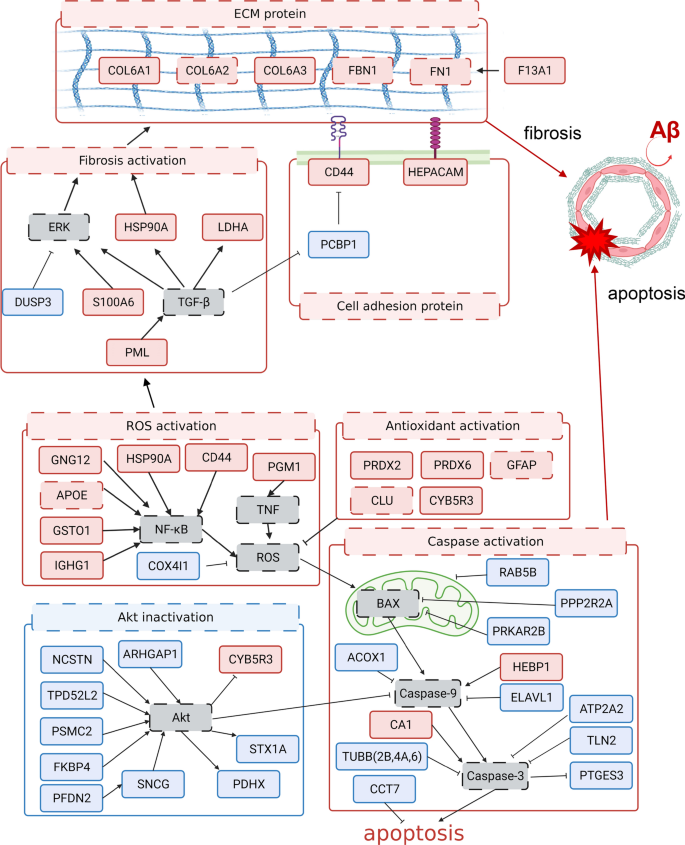
在与典型CAA标志物(Aβ或COL6A2)的相关性分析中,发现更多与脑毛细血管CAA病理相关的蛋白。在被量化的蛋白中,有56个蛋白满足以下两个条件:(1)在所收集的毛细血管中,6个ADNC +/CAA +和5个ADNC - /CAA -供体的平均表达水平差异超过1.5倍;(2)根据Spearman等级相关分析,在11个供体(6个ADNC +/CAA +和5个ADNC - /CAA -供体)中,与a β或COL6A2显著相关(p < 0.05)。在收集的10个供体(ADNC +/CAA -和ADNC - /CAA -组)的毛细血管中,只有13个蛋白与Aβ或COL6A2显著相关(p < 0.05)。这表明56个蛋白中超过70%是ADNC +/CAA +特异性致病蛋白。使用来自11个供体(ADNC +/CAA +和ADNC - /CAA -组)的数据进行相关性分析,在实质中,只有3种蛋白与Aβ或COL6A2显著相关,这表明56种蛋白中90%以上是血管特异性病理改变(表2)3.和附加文件2表2)。在这56种蛋白中,42种与纤维化、氧化应激和细胞凋亡有关。其中36个蛋白在本研究中首次被鉴定为在ADNC +/CAA +病理中表达水平发生变化的蛋白。基于这些发现,我们现在提出了ADNC +/CAA +血管中纤维化、氧化应激和凋亡激活的更详细的分子机制,如图所示。5.
CAA患者大脑皮质血管的假想分子机制。基于本研究结果,我们阐述了CAA患者大脑皮质血管发生的病理分子机制的特点。红色,在ADNC +/CAA +/H供体中显示显著上调或与Aβ或COL6A2显著正相关的蛋白。蓝色表示ADNC +/CAA +/H供体显著下调或与Aβ或COL6A2显著负相关的蛋白。灰色是在本研究中未被量化的蛋白质。本研究中首次明确的CAA毛细血管中蛋白表达有显著变化的蛋白用实线包围。在CAA毛细血管或CAA模型中已报道的蛋白表达变化的蛋白用虚线包围。单个分子的相互关系是基于我们的文献检索。本研究发现,包括ECM、粘附和TGF-β信号蛋白在内的多种纤维化通路分子被激活。此外,氧化应激相关分子的激活和AKT信号分子的失活也被发现,这可能激活了包括caspase信号在内的凋亡通路。 The activation of fibrosis and apoptosis leads to the suppression of the Aβ clearance and the destruction of cerebral vessels. Based on literature search, HSP90A, CD44, and CA1 are considered as therapeutic targets of taxifolin, verbascoside, and acetazolamide, respectively. The upregulation of these three proteins in CAA capillaries were clarified for the first time in the present study. The molecular mechanisms illustrated here would be useful for better understanding of the CAA pathology and for promoting the discovery and development of drugs and biomarkers for CAA
本研究结果表明,ADNC +/CAA +血管中纤维化被激活。COL6A2、FBN1和FN1的表达增加[8,9,10],而通过促进ECM合成而激活纤维化的TGF-β和ERK,在ADNC +/CAA +患者的脑血管中也有报道[11]。在本研究中,我们首次发现COL6A1, COL6A3和F13A1的表达(图2)。2),有助稳定流感病毒,则会增加[12]。我们还发现S100A6的表达增加[13],激活ERK,并降低DUSP3的表达[14],抑制ERK。此外,我们发现PML [15], hsp90a [16]及LDHA [17],它们是TGF-β信号的上游或下游,被上调。Taxifolin是目前作为ADNC +/CAA +的潜在治疗药物而备受关注的一种化合物。事实上,据报道,它具有多方面的作用,包括抑制Aβ低聚物的聚集,刺激它们从脑血管中清除,并通过抑制Nf-κB信号传导减少Aβ的产生[18,19]。然而,其在ADNC +/CAA +中的作用机制尚不完全清楚。据认为,血管中Aβ的清除会因纤维化而受损[20.]。因此,抑制纤维化可能会改善Aβ的清除[9]。有趣的是,据报道taxifolin可以抑制HSP90A的激活[21]。如图3所示。5,抑制HSP90A可抑制纤维化和Nf-κB信号的激活[22]。因此,taxifolin可能通过靶向ADNC +/CAA +中的HSP90A抑制纤维化和Nf-κB信号传导,从而增强Aβ清除并抑制其产生。
马鞭草苷作为ADNC +/CAA +的治疗剂也引起了人们的关注。据报道,当给予CAA模型小鼠时,它可以通过降低ROS水平来保护细胞免受氧化应激,并改善脑血管中Aβ的清除[23,24]。然而,关于保护细胞免受氧化应激和改善清除的分子机制的细节仍不清楚。在本研究中,CD44的表达增加[25]及HEPACAM [26],通过促进细胞- ecm粘附促进纤维化,并降低PCBP1的表达[27],抑制CD44,首次在ADNC +/CAA +患者的皮质血管中观察到(图2)。2).有趣的是,据报道毛蕊花糖苷可以抑制胶质母细胞瘤细胞系中CD44的活性[28]。因此,这些发现表明毛蕊花苷通过抑制CD44抑制纤维化。如上所述,抑制纤维化可提高Aβ的清除率。也有报道称,抑制CD44可抑制Nf-kB信号传导,从而抑制氧化应激[29]。因此,毛蕊花苷也可能靶向ADNC +/CAA +内皮细胞中的CD44,从而抑制纤维化和Nf-kB信号传导,改善Aβ清除并保护细胞免受氧化应激(图2)。5).
ADNC +/CAA +中APOE表达增加,激活Nf-κB信号通路促进ROS生成[8,30.]。GNG12表达增加[31], gsto1 [32]和IGHG1 [33],激活Nf-κB信号,并降低抑制ROS生成的COX4I1的表达[34],本文首次在ADNC +/CAA +患者的脑血管中得到证实(图2)。3.和5).也有报道称,与正常血液相比,ADNC +/CAA +患者血液中激活Nf-κB信号并增加ROS产生的LPS水平上调了三倍,并且LPS与脑血管中的Aβ共定位[35,36]。有趣的是,据报道,GSTO1的下调可显著减少lps刺激下ROS的产生[37]。因此,靶向抑制GSTO1可能具有治疗ADNC +/CAA +氧化应激诱导损伤的潜力(图2)。5).
在ADNC +/CAA +血管中,抗氧化蛋白(包括CLU和GFAP)的表达也有所增加。当这些蛋白质增加时,它们以细胞保护的方式对抗氧化应激。8,38,39,40]。在本研究中,我们首次发现抗氧化蛋白PRDX2和PRDX6表达增加[41],它们在氧化应激增加的情况下被上调,而CYB5R3 [42],它在AKT信号失活时被激活(图2)。3.和5), ADNC +/CAA +血管。这些蛋白表达的增加可能起到保护细胞免受氧化应激的作用(图2)。5).
对于AKT信号传导(图2)5),我们发现NCSTN [43], tpd52l2 [44], psmc2 [45], fkbp4 [46]及ARHGAP1 [47],激活AKT信号传导(图2)。4).PDHX的表达降低[48]及STX1A [49],它们被AKT信号激活,CYB5R3的表达增加[42],在ADNC +/CAA +血管中也出现了AKT信号失活激活的现象(图2)。4).这些结果表明AKT信号在ADNC +/CAA +血管中受到抑制(图2)。5).事实上,一项体外研究报道,暴露于Aβ使内皮细胞中AKT信号失活[50]。
有报道称,在ADNC +/CAA +中,BAX、caspase 3和caspase 9被激活并促进细胞凋亡(图2)。5) [1,51,52]。在本研究中,我们首次发现RAB5B [53],促进受损线粒体降解的PPP2R2A表达降低[54]抑制BAX,而PRKAR2B的表达[55,56]在ADNC +/CAA +患者的脑血管中,通过戊糖磷酸途径抑制BAX的表达减少(图2)。4).此外,HEBP1的表达增加[57]激活caspase 9,而ACOX1的表达降低[58],它们抑制caspase 9(图2)。4).TUBB2B, TUBB4A, TUBB6表达降低[59]及ATP2A2 [60]抑制caspase 3的作用,PTGES3的表达降低[61]受caspase 3的抑制,碳酸酐酶1 (CA1)的表达增加[62]激活caspase 3,也首次被展示出来(图2)。4).乙酰唑胺是一种CA1抑制剂,用于治疗癫痫和作为利尿剂,据报道,它可以抑制暴露于a β的人脑血管内皮细胞的凋亡[63]。虽然CA的抑制可能会抑制细胞凋亡,但在ADNC +/CAA +患者的脑血管中CA是否真的被激活的问题尚不清楚。本研究显示,ADNC +/CAA +血管中CA1的表达增加。这些结果表明,乙酰唑胺通过靶向诱导CA1的表达来抑制细胞凋亡(图2)。5).
在本研究中,LMD对血管进行了采样,除了内皮细胞外,还发现它们含有神经血管单位(NVU),如星形胶质细胞和周细胞;GFAP和CD44是星形胶质细胞标志物,在ADNC +/CAA +血管中表达升高,提示星形胶质细胞激活。周细胞产生胶原的能力更强,提示ADNC +/CAA +血管中COL6A1、COL6A2和COL6A3的增加是由于周细胞活化。然而,图中所示的许多分子。5是由内皮细胞、星形胶质细胞和周细胞表达的蛋白质类型。这使得仅根据本研究结果难以区分不同的细胞分子机制。在未来,为了阐明CAA如何整体影响NVU,将需要对NVU进行细胞特异性蛋白质组学分析。
在蛋白质组学分析中测量大量的读数增加了识别可能不真实的统计显著变化的机会。benjamin - hochberg (BH)修正可能会有所帮助,但这并不能完全解决这个问题。此外,当比较正在经历相同处理步骤的同一样品的两个实体的浓度时,检测到正关联的概率很高。因此,反向关联可能更有意义,因为没有这样的方法学偏差。无论如何,由于供体数量少,本研究报告结果的确定性可能不够。p值的标准设置为0.05,但0.01可能更合理的相关性分析。在未来,将需要使用更多供体样本的不同队列进行额外的定量分析。这将使本研究获得的结果更有可能是有效的。此外,还需要使用其他方法进行验证性实验。
将我们的蛋白质组学数据与之前CAA蛋白质组学研究报告的数据进行比较是很有趣的。在两项研究中,从CAA冷冻脑中分离出脑血管进行蛋白质组学分析,但在CAA血管中未检测到或未增加COL6A家族,而COL6A家族是直接参与纤维化的典型CAA病理[10,64]。CAA血管非常脆弱,在血管分离过程中血管结构被破坏。此外,并非所有使用的脑组织血管都必然表现出CAA病理(一些正常血管可能包括在样本中)。因此,这些研究报告的蛋白质组学数据可能不能充分反映CAA脉管系统的真实病理分子机制。2018年,再次使用LMD对CAA脑进行蛋白质组学分析,但血管未富集,基本切除包括血管在内的脑实质区域进行蛋白质组学实验[8]。虽然发现了COL6A家族的增加,但由于大多数细胞是实质细胞,因此没有充分捕获血管中的病理分子机制。我们解决了这些问题,并能够适当地量化CAA血管的病理分子机制。由于我们能够捕捉到与CAA中发生的纤维化、氧化应激和细胞死亡相关的蛋白质表达变化(图2)。5),我们得出结论,我们能够正确地阐明与CAA血管相关的病理分子机制。
FFPE切片在临床实践中得到了非常广泛的应用,在世界各地的医疗机构中已经收集和储存了大量标本,并附带了相关的临床信息。传统上,福尔马林交联一直是进行蛋白质组学实验的主要障碍。然而,我们能够开发一种基于pct的样品处理技术,该技术允许样品的完全去交联和胰蛋白酶消化,以及一种高度精确的基于swath的综合定量方法。这使我们能够通过使用这种FFPE切片来适当地量化体内发生的真实病理变化[3.]。预计该方法将在未来用于阐明与各种人类疾病相关的病理分子机制,而不仅仅是CAA,以及识别特定的生物标志物。
结论
结合基于lmd的FFPE切片血管分离、pct辅助样品处理和SWATH分析(FFPE- lmd - pct -SWATH方法),首次揭示了ADNC +/CAA +血管中参与纤维化、ROS产生和细胞死亡的许多蛋白的表达变化。ADNC +/CAA +显示HSP90A和CD44的表达增加,这是紫杉醇素和毛蕊花苷的治疗靶点。此外,我们首次发现CA1的表达增加,CA1是乙酰唑胺抑制ADNC +/CAA +细胞死亡的治疗靶点。我们期望在本研究中阐明的分子机制(图2)。5)将有助于更好地了解CAA的病理,并促进CAA药物和生物标志物的发现和开发。
数据和材料的可用性
支持本研究结果的数据可根据合理要求从通讯作者(Yasuo Uchida)处获得。
参考文献
张建军,张建军,张建军,等。caspase介导的β -淀粉样蛋白诱导脑微血管内皮细胞凋亡的研究进展。神经退行性疾病,2012;10(1-4):324-8。
李建军,李建军,李建军,李建军。脑淀粉样血管病在阿尔茨海默病的发病机制中起直接作用。支持caa的立场声明。中国生物医学工程学报。2004;25(5):589-97。
Uchida Y, Sasaki H, Terasaki T.基于相转移表面活性剂和swat - ms的热相容压力循环技术建立和验证高精度福尔马林固定石蜡包埋定量蛋白质组学。科学通报,2020;10(1):11271。
Montine TJ, Phelps CH, Beach TG, Bigio EH, Cairns NJ, Dickson DW,等。国家老年研究所-阿尔茨海默病协会阿尔茨海默病神经病理学评估指南:一种实用的方法。中华神经科杂志,2012;33(1):1 - 11。
Takao M, Hirose N, Arai Y, Mihara B, Mimura M.超级百岁老人的神经病理学-四个尸检案例研究。神经病理学杂志,2016;4(1):97。
散发性脑淀粉样血管病:病理、临床意义和可能的病理机制。中华神经科杂志,2005;11(4):345 - 359。
内田Y, Higuchi T, Shirota M, Kagami S, Saigusa D, Koshiba S,等。血浆蛋白、纤维连接蛋白和性激素结合球蛋白联合标志物预测子痫前期的鉴定和验证。中国生物医学工程学报,2011;44(6):804-15。
Hondius DC, Eigenhuis KN, Morrema THJ, van der Schors RC, van Nierop P, Bugiani M,等。蛋白质组学分析发现与阿尔茨海默病毛细血管淀粉样血管病相关的新标志物。神经病理学杂志,2018;6(1):46。
de Jager M, van der Wildt B, Schul E, Bol JG, van Duinen SG, Drukarch B,等。脑淀粉样血管病中组织转谷氨酰胺酶与细胞外基质蛋白共定位。中国生物医学工程学报,2013;34(4):1159 - 1169。
王晓明,李建平,李建平,等。老年和阿尔茨海默病伴脑淀粉样血管病的脑血管分子病理学研究。前沿老龄神经科学,2021;13:658605。
李建军,马洛里,李建军,李建军,等。细胞因子tgf - β 1在转基因小鼠和阿尔茨海默病中的淀粉样变性作用大自然。1997;389(6651):603 - 6。
Myneni VD, Hitomi K, Kaartinen MT.转谷氨酰胺酶因子XIII-A在前脂肪细胞增殖和分化之间起开关作用。血。2014;124(8):1344 - 53年。
夏鹏,何宏,Kristine MS,关伟,高军,王铮,等。重组人S100A6和可溶性晚期糖基化终产物受体(sRAGE)对ccl4诱导小鼠肝纤维化的治疗作用。中华药理学杂志,2018;33(3):86 - 93。
王晓明,王晓明,王晓明,等。双特异性磷酸酶VHR在T细胞抗原受体和cd28诱导的Erk和Jnk活化中的抑制作用。中国生物医学工程学报,2009;27(7):444 - 444。
刘勇,赵东,邱峰,张丽丽,刘世凯,李云云,等。通过沉默UBC9和RNF4调控PML summoylation调节心脏纤维化。生物化学学报,2017;25(3):666-78。
Sontake V, Wang Y, Kasam RK, Sinner D, Reddy GB, Naren AP,等。Hsp90对肺纤维化成纤维细胞活化的调控。JCI Insight, 2017;2(4): e91454。
Soukupova J, Malfettone A, Hyrossova P, Hernandez-Alvarez MI, penuela - haro I, Bertran E,等。转化生长因子- β在调节肝癌氧化代谢中的作用。科学通报,2017;7(1):12486。
引用本文:朴世英,金海燕,金海军,辛洪,洪广华,金德成。紫杉醇和西洛他唑同时治疗对P-JAK2/P-STAT3/NF-kappaB/BACE1信号通路的抑制作用及β -淀粉样蛋白积累的影响。PLoS ONE。2016; 11 (12): e0168286。
田中平,张建平,李建平,等。脑淀粉样蛋白血管病变的临床研究进展。中华医学杂志,2011;12:643357。
韦勒RO,普雷斯顿SD,苏巴什M,卡拉雷RO。脑淀粉样血管病在阿尔茨海默病的病因学和免疫治疗中的作用。老年痴呆症杂志,2009;1(2):6。
李建军,张建军,张建军,等。紫杉醇蛋白对细胞凋亡的分子动力学模拟研究。[J] .中国生物医学工程学报,2012;37(3):327 - 338。
Thangjam GS, Birmpas C, Barabutis N, Gregory BW, Clemens MA, Newton JR等。Hsp90抑制通过Sirt-2抑制人肺微血管内皮细胞NF-kappaB转录激活。[J] .中华医学杂志,2016;31(10):964 - 974。
kakotskaia D, Agca C, Richardson RA, Stopa EG, Schachtman TR, Agca Y. APP+PS1双转基因大鼠阿尔茨海默病模型的记忆缺陷、脑淀粉样蛋白血管病变和淀粉样蛋白斑块。PLoS ONE。2018; 13 (4): e0195469。
王超,蔡鑫,王锐,翟松,张勇,胡伟,等。毛茛苷通过缓解β暴露的U251细胞和APP/PS1小鼠内质网应激对阿尔茨海默病的神经保护作用中华神经科杂志,2010;17(1):39。
Rouschop KM, Sewnath ME, Claessen N, Roelofs JJ, Hoedemaeker I, van der Neut R,等。CD44缺乏增加梗阻性肾病的肾小管损害,但减少肾纤维化。中国生物医学工程学报,2004;15(3):674-86。
莫丽娟,张超,罗超,李丽华,沈思。一种新型igg样细胞粘附分子hepaCAM在人乳腺癌MCF7细胞中的结构和功能分析。生物化学学报,2005;29(2):368 - 368。
张涛,黄晓华,董磊,胡东,葛超,詹玉青,等。PCBP-1调节CD44基因的选择性剪接并抑制人肝癌细胞系HepG2细胞的侵袭。癌症杂志。2010;9:72。
王超,王忠,陈超,付旭,王杰,费旭,等。一种低分子量CD44二聚化抑制剂治疗胶质母细胞瘤。中国生物医学工程杂志,2011;32(3):444 - 444。
Qadri M, Almadani S, Jay GD, Elsaid KA。CD44在调节人巨噬细胞TLR2激活和促炎细胞因子下游表达中的作用。中华免疫学杂志,2018;20(2):758-67。
张建军,张建军,张建军,张建军。淀粉样蛋白β诱导氧化应激介导的毛细血管淀粉样血管病血脑屏障改变。抗氧化还原信号。2011;15(5):1167-78。
李军,金超,邹超,乔霞,马鹏,胡东,等。GNG12通过激活NF-kappaB信号通路调节胰腺导管腺癌中PD-L1的表达。生物工程学报。2020;10(2):278-87。
Menon D, Coll R, O 'Neill LA, Board PG.巨噬细胞中脂多糖刺激诱导NADPH氧化酶1和产生活性氧所必需的谷胱甘肽转移酶- 1。中华生物医学工程学报,2014;33(3):391 - 391。
王静,林丹,彭辉,邵军,顾军。癌源性免疫球蛋白G通过与TLR4结合促进lps诱导的宫颈癌细胞促炎细胞因子的产生。Oncotarget。2014;5(20):9727 - 43。
Leadsham JE, Sanders G, Giannaki S, Bastow EL, Hutton R, Naeimi WR等。细胞色素c氧化酶的缺失促进了酵母内质网内NADPH氧化酶Yno1p产生ras依赖的ROS。中华医学杂志,2013;18(2):279-86。
张晓峰,张晓峰,张晓峰,等。脂多糖与阿尔茨海默病脑内淀粉样斑块、神经元和少突胶质细胞的关系研究进展。神经科学进展,2018;10:42。
詹晓霞,金立文,陈建军,陈建军。革兰氏阴性细菌与阿尔茨海默病的关系。神经学。2016;87(22):2324 - 32。
Menon D, Innes A, Oakley AJ, Dahlstrom JE, Jensen LM, Brustle A,等。GSTO1-1在炎症、结肠炎和肥胖模型中发挥促炎作用。科学通报,2017;7(1):17832。
奥瓦西尔R, O 'Neill R, Keable A, Nimmo J, MacGregor Sharp M, Kelly L,等。AQP4在人脑衰老和脑淀粉样血管病中的表达模式。中华医学杂志,2020。https://doi.org/10.3390/ijms21041225.
唐松,叶松,马燕,梁燕,梁宁,肖峰。聚簇素通过抑制Ca(2+)- ros - drp1 -线粒体裂变轴减轻Cr(VI)诱导的L02肝细胞线粒体凋亡。中国生物医学工程学报,2014;33(2):444 - 444。
张松,吴敏,彭超,赵刚,顾瑞。GFAP在大鼠损伤星形胶质细胞中的表达。中华医学杂志,2017;14(3):1905-8。
Diet A, Abbas K, Bouton C, Guillon B, Tomasello F, Fourquet S,等。免疫刺激巨噬细胞中一氧化氮对过氧化物氧化素的调节。生物化学学报,2007;32(5):391 - 391。
Siendones E, SantaCruz-Calvo S, Martin-Montalvo A, Cascajo MV, Ariza J, lopez - luch G,等。膜结合的CYB5R3是通过FOXO3a和Nrf2参与营养和氧化应激反应的常见效应因子。抗氧化还原信号。2014;21(12):1708-25。
王翔,王翔,徐毅,闫敏,李伟,陈杰,等。nicastrin通过PI3K/AKT信号通路调节对肝癌细胞增殖和凋亡的影响。中华肿瘤杂志,2020;20:91。
陈强,王鹏,付勇,刘霞,徐伟,魏军,等。MicroRNA-217通过靶向Tpd52l2抑制人胰腺腺癌细胞增殖、侵袭和迁移。中国生物医学工程学报,2017;38(6):3567-73。
陈强,傅丽,胡军,郭刚,谢安。PSMC2基因沉默通过调控前列腺癌的增殖、凋亡和迁移抑制前列腺癌的发生和转移。中华肿瘤杂志,2011;21(1):35 - 35。
孟伟,孟军,姜宏,冯鑫,魏东,丁强。FKBP4通过激活Akt/mTOR信号通路加速非小细胞肺癌的恶性进展。肛门细胞病理学杂志,2020;2020:6021602。
杨超,张刚,张勇,张生,李军,刘勇。外泌体miR-134-5p通过靶向ARHGAP1调控PI3K/AKT通路抑制乳腺癌进展。中华妇产科杂志;2011;47(11):4037-48。
邓伟,刘宏斌,陈毅,陈永华,Epperson CM,姜超,等。蛋白激酶B (PKB/AKT1)与线粒体蛋白形成信号复合物,并在缺血再灌注损伤时阻止培养心肌细胞糖酵解能量功能障碍。内分泌学。2014;155(5):1618 - 28。
刘敏,张宏,张强,黄超,史旭。Syntaxin 1A介导异氟醚而非缺氧预处理诱导的大鼠心肌细胞缺氧再氧化损伤。[J] .地理学报,2015;7(10):1883-95。
尹建军,李建明,陈华,徐军,徐永春。Abeta25-35改变Akt活性,导致脑血管内皮细胞不良易位和线粒体功能障碍。[J]中华血液学杂志,2009;25(11):444 - 444。
徐美娟,徐永春,陈宝林,陈曼敏,欧刚,林长春。淀粉样蛋白肽诱导脑内皮细胞凋亡的信号调节激酶1。中华神经科学杂志。2007;27(21):5719-29。
Mok SS, Turner BJ, Beyreuther K, Masters CL, Barrow CJ, Small DH。同型半胱氨酸可增强底物结合淀粉样肽对血管平滑肌细胞的毒性。中国生物医学工程学报,2009;32(1):444 - 444。
Hammerling BC, major RH, Cortez MQ, Shires SE, Leon LJ, Gonzalez ER,等。Rab5内体途径介导帕金森依赖性线粒体清除。学报。2017;8:14050。
李翔,姚翔,谢宏,张刚,邓明,邓康,等。PPP2R2A通过调节湖羊子宫内膜基质细胞增殖和凋亡影响胚胎着床。以及动物生殖部。2021;技术部176:149 - 62。
尹浩,张浩,金永英,文顺,李顺,赵敏,等。PRKAR2B的敲低导致卵母细胞成熟失败。细胞生理与生物化学,2018;45(5):2009-20。
谢宝宝,黄立文,苏世杰,程海龙,胡玉春,洪振东,等。精氨酸和抗坏血酸联合处理可诱导肝癌细胞系HA22T/VGH细胞凋亡,并改变戊糖磷酸途径及活性氧和活性氮的氧化还原状态。生物化学学报,2011;22(3):234-41。
Yagensky O, Kohansal-Nodehi M, Gunaseelan S, Rabe T, Zafar S, Zerr I,等。阿尔茨海默病早期血红素结合蛋白1的表达增加与神经毒性有关。Elife》2019。https://doi.org/10.7554/eLife.47498.
郑调峰,陈文博,秦涛,吕林宁,冯斌,陆玉玲,等。ACOX1破坏p73的稳定性,抑制淋巴瘤细胞的内在凋亡途径并调节对阿霉素的敏感性。中国生物医学工程学报,2019;52(9):566-71。
赵玲,罗生,徐强,张波。微管蛋白偶联死亡受体5调控细胞凋亡。Oncotarget。2018;9(95):36804 - 15所示。
王丽,王丽,宋睿,沈艳,孙艳,顾艳,等。姜黄素靶向肌浆/内质网Ca(2)+- atp酶2诱导内质网应激相关凋亡治疗人脂肪肉瘤中华肿瘤杂志,2011;10(3):461 - 471。
Mollerup J, Berchtold MW。共伴侣蛋白p23在细胞凋亡过程中被半胱天冬酶和蛋白酶体降解。生物化学学报。2005;579(19):4187-92。
刘霞,陆东,鲍泽瑞,刘军。肌萎缩侧索硬化症患者运动神经元中碳酸酐酶I的表达及变化。中华医学杂志,2016。https://doi.org/10.3390/ijms17111820.
Solesio ME, Peixoto PM, Debure L, Madamba SM, de Leon MJ, Wisniewski T等。碳酸酐酶抑制选择性地防止淀粉样蛋白神经血管线粒体毒性。老化细胞,2018;17(4):e12787。
Zellner A, Muller SA, Lindner B, Beaufort N, Rozemuller AJM, Arzberger T,等。脑淀粉样血管病的蛋白质组学分析显示与CADASIL重叠,突出HTRA1及其底物的积累。神经病理学杂志,2022;10(1):6。
致谢
作者希望感谢Milton S Feather博士(美国的科学编辑)对整个手稿进行英文校对。
资金
本研究得到了日本科学促进会(JSPS)科学研究补助金(B) [KAKENHI: 20H03399],促进国际联合研究(A) [KAKENHI: 18KK0446]和挑战性研究(探索性)[KAKENHI: 21K19365]的部分支持。本研究还得到了教育、文化、体育、科学和技术省(MEXT)为创新领域科学研究提供的部分资助[KAKENHI: 22H04798, 20H05495和20H04690],并得到了武田科学基金会和日本癫痫研究基金会的部分支持。本研究还得到了日本医学研究与开发机构(AMED)的部分资助[资助号:22dk0207063s0101和JP21wm0425019]、JST进化科学与技术核心研究(crest)资助[资助号:JPMJCR17H1]和国家神经病学和精神病学中心的内部基金[资助号:3-8]。
作者信息
作者及单位
贡献
TH:进行实验,分析/获取数据,研究设计/构思,起草手稿。方法开发。MT和MT:提供人脑组织。YU:论文的起草,论文的修改,研究的设计/构思,数据的分析/获取。所有作者都阅读并批准了最终的手稿。
相应的作者
道德声明
伦理批准并同意参与
所有参与者按照当地机构审查委员会(IRB)的要求提供知情的书面同意,并符合赫尔辛基宣言及其修正案。
发表同意书
不适用。
相互竞争的利益
没有竞争利益需要申报。
额外的信息
出版商的注意
beplay體育施普林格·自然对已出版的地图和机构关系中的管辖权要求保持中立。
补充信息
附加文件2:表S1。
孤立毛细血管和薄壁组织的原始SWATH数据。表S2。Spearman 's rank相关性与COL6A2提取caa特异性和血管特异性病理改变。
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议,该协议允许以任何媒介或格式使用、共享、改编、分发和复制,只要您适当地注明原作者和来源,提供知识共享许可协议的链接,并注明是否进行了更改。本文中的图像或其他第三方材料包含在文章的知识共享许可协议中,除非在材料的署名中另有说明。如果材料未包含在文章的知识共享许可中,并且您的预期用途不被法律法规允许或超过允许的用途,您将需要直接获得版权所有者的许可。如欲查阅本许可证副本,请浏览http://creativecommons.org/licenses/by/4.0/.创作共用公共领域免责声明(http://creativecommons.org/publicdomain/zero/1.0/)适用于本文中提供的数据,除非在数据的信用额度中另有说明。
关于本文
引用本文
韩田,T.,佐佐木,H.,高雄,M.。et al。基于蛋白质组学的FFPE-LMD-PCT-SWATH方法研究脑淀粉样血管病脑血管分子机制。流体屏障19, 56(2022)。https://doi.org/10.1186/s12987-022-00351-x
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/s12987-022-00351-x
关键字
- 创新艺人经纪公司
- 纤维化
- 一个β
- 细胞凋亡
- 片