摘要
本文综述了脑脊液(CSF)循环动力学的八个方面:形成速率、压力、流量、体积、周转beplay靠谱率、成分、循环和重吸收。最近对脉络膜丛转录因子(E2F5)、离子转运体(NaHCO)的分析提出了调节脑脊液形成的新方法3.共转运),转运酶(碳酸酐酶的异构体),水通道蛋白1调节,以及液体调节神经肽受体的可塑性。对脑脊液压力(CSF pressure, CSFP)有了新的认识,包括肽能调节伺服机制、功能失调的室管膜和脑室周围器官在导致先天性脑积水中的作用,以及临床应用算法来描绘ccsf波形以用于诊断和预后。越来越多的关注集中在脑脊液流动:它如何影响脑代谢和血流动力学,脑室下区神经干细胞的进展,以及中枢神经系统分解代谢物/肽的清除。从血流动力学(脉络膜丛血流和搏动)、流体动力学(脉络膜低分泌和高分泌)和神经内分泌因子(即心房利钠肽、精氨酸加压素和碱性成纤维细胞生长因子的协同调节)的角度评估脑脊液容积变化的病理生理意义。在衰老、常压脑积水和阿尔茨海默病中,脑脊液空间的扩大降低了脑脊液的周转率,从而影响了脑脊液清除中枢神经系统有害代谢物(如淀粉样蛋白)的作用。脑脊液动力学减弱严重损害神经元间质环境。因此,神经退行性疾病和衰老中脑脊液成分的改变,由于对神经过程和认知的不利影响,需要更有效的临床管理。蛛网膜下腔、脑和脑室之间的脑脊液循环促进间质液(ISF)对流,具有营养和排泄的双重好处。最后,当CSF fp和液体潴留明显升高时,脑脊液通过多种途径(嗅觉和脊髓蛛网膜大流量)重吸收可能通过毛细血管壁(水通道蛋白4)和蛛网膜绒毛的液体清除来补充。提出了一个模型,将CSF和ISF稳态与血-CSF和血-脑运输界面的水和溶质的协调通量联系起来。
大纲
1概述
2脑脊液的形成
2.1转录因子
2.2离子转运体
2.3调节运输的酶
2.4水通道或水渠
2.5神经肽受体
3脑脊液压力
3.1伺服机制调节假说
3.2脑脊液压力产生的个体发生
3.3先天性脑积水和脑室周围区域
3.4脑对脑脊液压力升高的反应
3.5脑脊液波形测量的进展
4脑脊液流量
4.1脑脊液流量与脑代谢
4.2流动对胎胚基质的影响
4.3老化中枢神经系统CSF流量减少
4.4改进无创流量测量
5脑脊液容积
5.1血流动力学因素
5.2水动力因素
5.3神经内分泌因素
6 CSF周转率
6.1脑室肿大的不良影响
6.2减弱的脑脊液汇作用
7 CSF成分
7.1 CP-CSF系统的肾样作用
7.2衰老和疾病时脑脊液生化改变
7.3清关运输的重要性
7.4成分的治疗性操作
CSF循环与ISF动力学的关系
8.1脑间质脑脊液交换
8.2脑内ISF运动的组成
8.3 ISF/CSF动力学和淀粉样蛋白保留受损
9脑脊液重吸收
9.1蛛网膜流出阻力
9.2蛛网膜绒毛与嗅觉引流途径
9.3沿脊神经的液体重吸收
9.4毛细水通道的重吸收
10建立恢复脑脊液平衡的翻译有效模型
11的结论
1概述
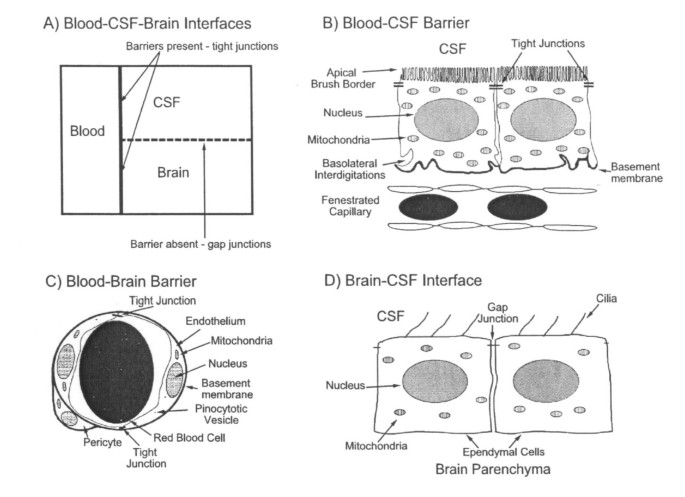
自由流动的脑脊液(CSF)beplay靠谱成分受到良好调节,对大脑健康至关重要[1,2].衰老或疾病引起的脑脊液循环改变对神经元功能有不利影响[j]。2,3.].终其一生,脉络膜丛(CP)-脑脊液动力学可因肿瘤、感染、创伤、缺血或脑积水而受损。4- - - - - -8].脑脊液流动严重中断会扰乱认知和运动功能[9].如果关键的脉络膜-脑脊液参数被扭曲,中枢神经系统的活力就会受到损害。对于健康和疾病来说,描述脑脊液与脑脊液之间的相互作用是至关重要的。1).
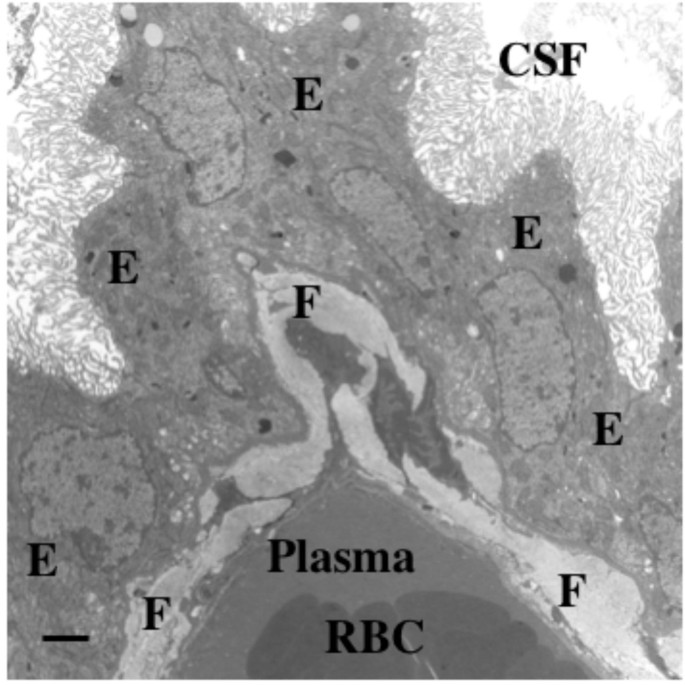
血-脑- csf界面形态:(A)中枢神经系统主要隔室及接口示意图。血脑屏障和血csf屏障分别是内皮细胞和上皮细胞之间紧密连接的真正屏障。由于室管膜(或神经胶质)细胞之间的间隙连接,脑- csf界面比脑或脊髓毛细血管和脉络丛更具渗透性。(B)血- csf屏障。CP由一层呈周状排列的上皮细胞组成。与大脑的毛细血管不同,神经丛毛细血管可以渗透大分子。(C)血脑屏障:内皮细胞紧密连接,细胞旁通透性低。内皮细胞胞饮性囊泡缺乏反映胞吞作用极少。(D)脑-CSF界面:侧脑室室管膜衬里允许溶质在脑ISF和大腔脑脊液之间相对自由地扩散。室管膜细胞顶端的活动纤毛将CSF向下游移动至SAS。 Reprinted with permission from高级给药审查[17].
改进的生物技术和模型现在可以精确地评估CP-CSF在调节大脑发育,代谢和衰老中的作用[qh]10- - - - - -12].替代移植[13- - - - - -15]和药理学策略[16- - - - - -18使用CP可能有助于挽救衰弱的脑脊液系统。这种纠正脑脊液参数的治疗最终将有利于神经网络功能。这篇综述提出了在疾病中稳定脑脊液或在晚年抑制其恶化的新方法[19].
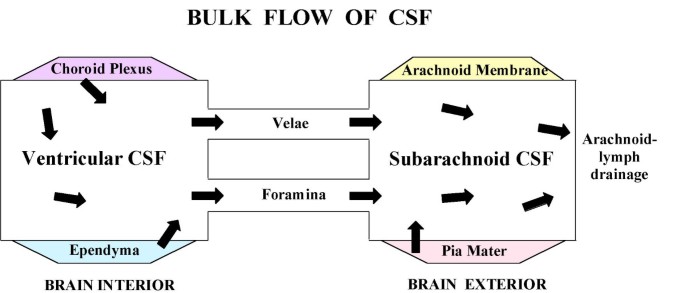
CSF评估应综合考虑物理、生化和生理参数(表1)1).此外,大腔脑脊液系统是多室的(图2)。2).脑室、脑池和蛛网膜下腔(SAS)是串联的。上游CSF转运现象对下游产生影响。脑脊液在功能上与室管膜壁相互作用[1]以及更深层的脑毛细血管表面[16,17].扩散和体积流动促进溶质和水在脑内和脑外的分布,这取决于各隔室中普遍存在的浓度和静水压力区域梯度。1).因此,分析中枢神经系统的液体空间是相关的——它们是如何被心室功能障碍破坏的,并可能被csf传播的治疗药物所改变。这将促进脑脊液在神经退行性疾病和其他疾病中的转化步骤。
大腔脑脊液室和大流量。细胞外液使液体从心室向SAS的体积传输(对流)成为可能[7,27]。脑脊液形成外侧,3理查德·道金斯和图4th心室CPs从外侧流向3理查德·道金斯心室通过脑导水管和4th脑室至大池SAS。然后脑脊液通过池孔(Magendie和Luschka)以大流量传输到基底池。脑脊液也从脑室通过瓣通道向四合体和周围池传导[167]。此后,液体被对流到脊髓的SAS和脑凸起处。当脑脊液流经脑室-蛛网膜下腔系统时,脑脊液与脑之间存在弥漫性和大量流动交换[16,24,168,169,289],这取决于特定区域的浓度梯度和静水压力,从而促进脑脊液携带物质的广泛分布[255]。正常情况下,脑脊液很容易从脑室分布到蛛网膜引流处。在脑积水中,血流通路可在多个点中断。
2脑脊液的形成
几个中枢神经区形成CSF或CSF样液体。虽然CP组织产生了约三分之二的总产生量,但脉络膜外来源弥补了平衡[20.].血脑屏障(BBB)中的毛细血管-星形胶质复合体被认为是脑间质液(ISF)的活跃生产者[21],但其速率通常比血脑脊髓液屏障BCSFB慢得多(按屏障表面积归一化时为1/100)[beplay靠谱22].血脑屏障是流体发生器的假设虽然很有吸引力,但需要证实。根据Pollay和Curl的说法,脑脊液的另一个可能来源是脑室的室管膜[23].蛛网膜虽然分泌多肽和蛋白质,但其表面积相对较大[24],可能不会主动形成CSF。因为CP在中枢神经系统内迅速产生大部分流体,并且已被广泛记录为csf形成能力[1],下面主要讨论脉络膜上皮。
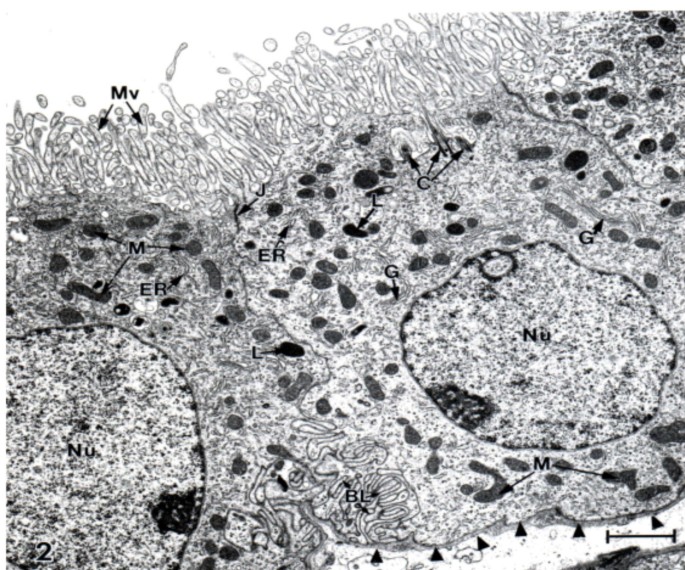
新生脑脊液起源于脑室内部,由侧脑脊液不断产生理查德·道金斯和图4th心室。由于中枢神经系统代谢受脑脊液转运的深刻影响,因此有必要描述脑脊液分泌的生理和分子过程。脑脊液的形成分为两个阶段:液体被动滤过脉络膜毛细血管内皮[25],然后通过单层上皮进行调节的活性分泌(图2)。3.).大量的研究表明溶质通过扩散、便利运输和主动运输从血液到脑脊液的运动。这些研究阐明了跨BCSFB流体传输的性质和独特性。
脉络膜丛上皮(CPe)细胞以高容量产生液体[1].CPe分泌引擎是由活跃的有机底物和水输入到广泛的毛细血管丛的小动脉驱动的[1].在哺乳动物中,约4ml /min/g CP的血流转化为约0.4 ml/min/g的脑脊液。已量化的形成率最小的哺乳动物是小鼠,其产生CSF的速率为3.3 × 104毫升/分钟(26].如果根据每体积脑组织产生的脑脊液将动物数据外推到人类,则人类脑脊液的产生应约为0.8 ml/min。然而,迄今为止的测量表明,人类脑脊液的产量大约是这个比率的一半[3.].
脑脊液的形成始于血浆通过可渗透脉络膜毛细血管过滤[25].净过滤与血液和脉络膜间质液(ISF)之间的静水压梯度成正比。正常情况下,根据斯特林滤过定律,液体自由地从血浆流入上皮细胞基底外侧表面的ISF。通过速率受限的组织灌注减少了神经丛的血流量,减少了血浆进入间质的滤过。因此,在急性脑积水中,脑脊液压力的显著升高,当向脉络膜ISF逆行传递时,减少了向ISF的血浆渗出。这减少了脑脊液的形成。然而,在正常的脉络膜灌注和脑脊液流体动力学下,血浆超滤液(离子和水)的连续流被呈现出来,用于向上皮基底外侧的转运体制造液体。
水、离子和大分子的经脉络膜分泌驱动脑脊液的体积传递(图2)。2)沿脑室-脑池轴向下[27].主动形成的脑脊液源于溶质在薄上皮界面上的协调分泌(图2)。3.)内脉络膜血浆和外心室液之间。CP上皮在结构上呈极化(图2)。3.)和功能(图2)。4和5).脑脊液动力学的药理学建模必须建立在神经丛血流以及上皮代谢和运输的基础知识之上。5).
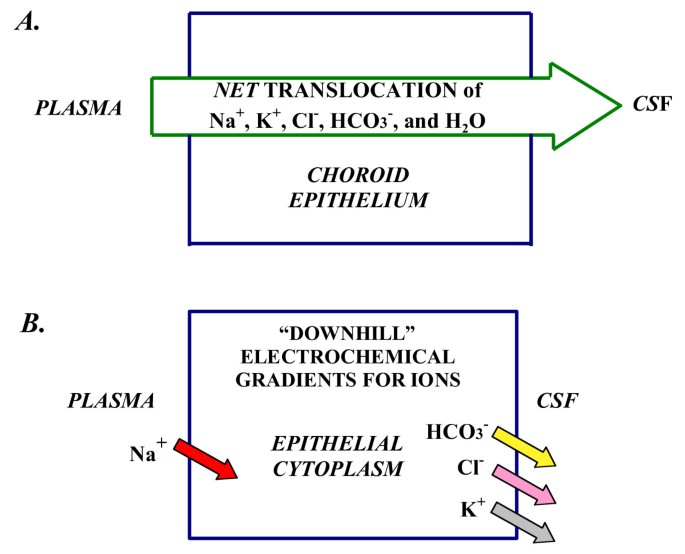
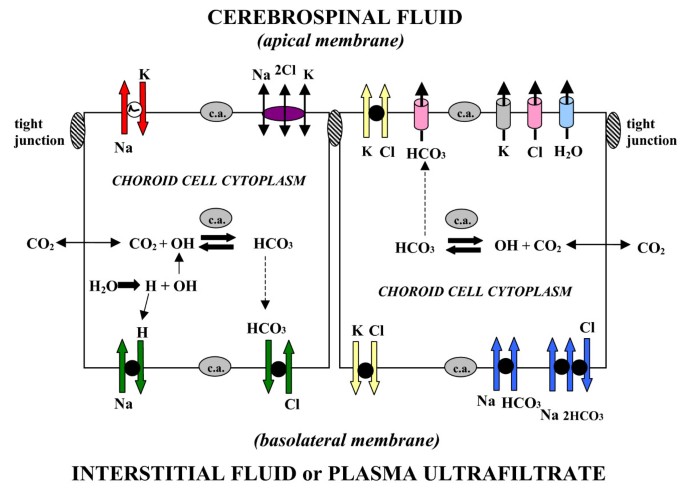
脑脊液形成机制:净离子传输和电化学梯度A. CP分泌脑脊液是通过Na的净传输+K+, Cl-, HCO3.-还有水,从血浆到心室。脑脊液对血液的再吸收离子通量与活跃的分泌同时发生,但总的来说,离子和水进入脑室是净运动的。脑脊液渗透压类似血浆。b . Na+通过二次主动转运(如钠)沿浓度梯度向下移动+- h+基底外侧膜交换)(图5)[38,43]。K+, Cl-和HCO3.-通过顶膜中的离子通道[50]沿电化学梯度扩散[38](图5)。箭头表示Na+象征着一个陡峭的向内浓度和电化学梯度[38]。K+, Cl-和HCO3.-,箭头分别描绘了向外的电化学梯度,促进离子通过通道扩散到脑脊液[50]。钠的脉络膜细胞浓度(mM)+K+, Cl-和HCO3.-,大鼠分别约为48、145、65和9.5[38]。CPe膜之间的电位差为45-50 mV,在pH 7.4时脑脊液对血浆呈阳性约5 mV。
哺乳动物脉络膜上皮中的离子转运体和通道。典型的CPe被描述为定位离子和水的转运体和通道[290]。脑脊液的分泌是由于离子和水从基底外侧膜协调运输到细胞质,然后依次穿过顶膜进入脑室。在质膜上有平行的钠离子+- h+和Cl--HCO3.-交换[38]带来Na+和Cl-进入细胞以换取H+和HCO3.-,分别。同样位于基底侧的是Na+-HCO3.-共转运(NBCn1)[41]和na依赖性Cl--HCO3.-交换物[42]调节pH,可能还调节脑脊液的形成。顶端Na+泵送[49,110]维持低细胞钠+形成一个有利的基底侧梯度来驱动钠离子+吸收。Na+主要通过Na+泵[110],在某些条件下,Na+- k+2氯-转运蛋白[46]。K+cl-共转运有助于维持细胞体积[50]。顶端通道促进K+, Cl-和HCO3.-扩散到脑脊液[68]。面向csf膜上的水通道蛋白1通道[77]介导进入脑室的水通量。碳酸酐酶和Na的极化分布+- k+- atp酶[51]和水通道蛋白使净离子和水转运到脑脊液。
脑脊液的形成涉及CPe中一系列复杂的转运蛋白和通道。这一复杂过程中的突出因素值得强调。因此,无花果。4图示脉络膜上皮极性(侧边性)如何与溶质跨BCSFB的细胞运动相关。虽然离子的双向运输发生在脉络膜上皮细胞的两极,但脑脊液的形成本质上是Na的净运输+, Cl-K+, HCO3.-水从血浆到CP再到CSF(图2)。4).离子和水通过基底侧膜的促进机制被吸收,通过细胞质对流,然后释放或主动分泌到顶侧脑室。在方向上,Na存在有利的电化学梯度(能量下坡)+在等离子体一侧向内运动对于K+, Cl-和HCO3.-脑脊液侧向外扩散(图2)4 b).通过水通道蛋白(AQP)通道促进的水通量渗透平衡了集体离子运输并为脑脊液循环提供了介质。
脑脊液的生成是脑液内稳态的主要特征[1].脑脊液形成速率的精细控制是脑液相关疾病治疗的一个挑战。历史上,重点一直放在发现新的药物来缓解脑脊液压力升高(CSFP),即颅内压(ICP),在儿童脑积水患者。预测指出,增加老年患者脑脊液周转率的额外迫切需要,因为许多人正在服用利尿剂和洋地黄制剂,以减少脑脊液的形成。这意味着更广泛的脑脊液药理学。为了个体化治疗常压和高压脑积水,应该有一个药物库来上调和下调脑脊液形成率。
随着细胞机制的阐明,通过CP修饰脑脊液产生的药理靶标将得到进一步的研究。迄今为止,乙酰唑胺和速尿是仅有的几种在控制脑脊液形成和颅内压方面具有临床应用价值的药物,但其副作用限制了它们的使用[28,29].显然,需要新的药物来恢复因疾病和损伤而改变的脑脊液动力学。理论上,核、细胞质和质膜成分是加速或减少脑脊液产生的药物作用的潜在位点。细胞核中的转录因子、细胞质中的酶以及质膜上的转运体/通道和受体都是潜在的药物靶点。修改脑脊液形成率的五种方法,即前沿和成熟的方法,概括在表中2详细说明如下:
2.1转录因子
传统上,脑脊液的形成是通过干扰膜离子转运体或减少底物的递送来改变的。然而,调节脑脊液分泌的代谢上游分子操作值得考虑。一种新的方法是靶向转录因子作为脑脊液形成过程中细胞酶的假定调节因子。缺乏转录因子p73、foxJ1和E2F5的小鼠发生非阻塞性脑积水[30.,31],可能由脑脊液分泌过多引起。上皮细胞超微结构分析和显微镜下的电子半透明与CP加速流体形成一致[j]。32].有趣的是,CPe中的E2F5随着细胞成熟(即从假层上皮转变为单立方上皮)而下调其产生CSF的能力[30.].这些在小鼠和人CP中转录因子的个体发生研究发现[30.,31提示一种通过操纵E2F5表达来增加CSF形成的新方法。
释放对脑脊液制造的自然抑制制动将是一种独特的方式来增加流体在脑脊液上的转移。这种理论方法有一个实验先例。切除颈上神经节交感神经可减弱CP上的抑制性自主神经张力,从而增加脑脊液的产生[32].增强脑脊液的形成和相关的汇作用[33脑间质溶质的研究可能适用于衰老、常压脑积水(NPH)和阿尔茨海默病(AD)患者,这些患者因液体周转缓慢而保留细胞外代谢物[qh]19].
2.2离子转运体
大多数调节脑脊液形成速率的尝试都是针对改变脑脊液基底外侧(面向血浆)和根尖(面向CSF)膜上转运蛋白的离子运动[1].因为CP是肾型器官[34],有上皮机制[35]与肾小管中传输大量离子和水的利尿剂类似,许多利尿剂已被测试具有抑制脑脊液形成的能力[1,27].了解CPe中的许多离子转运体和通道是实现脑脊液产生的精细控制、上调和下调的关键。
在基底外侧膜,钠的摄取+和Cl-是脑脊液形成的首要步骤(图2)。5).向内传递固定离子Na+和Cl-这是由载体在功能上依赖于钠的基底外侧跨膜梯度来促进的+, Cl-H+和HCO3.-。基底外侧Na+- h+交换剂(NHE1)将Na转移到脉络膜细胞中。这一过程被利尿剂阿米洛利所抑制[36- - - - - -38],减少脑脊液的形成[36,38].这种作用类似于抑制近端和远端小管钠引起的多尿+- h+通常支持肾脏大量液体转移的交换器(NHE3) [39].的Cl--HCO3.-交换器转运间隙Cl-进入细胞质。此外,基底外侧Na+端依赖Cl--HCO3.-交换剂和Na+-HCO3.-CPe共转运体[40- - - - - -42]也可能是控制流体运动的潜在目标。Na+与HCO耦合3.-运输可能是新生脑脊液生成不可或缺的一部分[43,44].与代谢性酸中毒相比,全身性代谢性碱中毒会促进Na的产生+流入CPe,随后流入脑脊液[38].因此是基底外侧HCO3.-运输(40,42]通过一种或多种机制(图2)。5)可能被操纵来修饰HCO3.-改变或改变脉络膜细胞的pH值以调节流体的形成。
在顶膜Na处+- k+- atp酶,钠泵,是一个主动将钠分泌到心室的主力军(图2)。5),从而推动脑脊液的形成。钠泵将细胞钠保持在低水平[38]通过Na共转运体为基底外侧向内移动的Na建立驱动力(有利梯度)。因此,通过扭曲跨膜离子梯度对根尖钠泵的药理学破坏,继发地使对侧基底面转运活性丧失。位于顶端的Na+- k+2氯-协同转运蛋白(NKCC1)在双向转运能力方面具有重要意义。共转运体在分泌和重吸收两种模式下转移离子的能力[45反映了调节细胞离子稳态和脑脊液动力学的多功能转运体。布美他尼对NKCC1活性的干扰46]或速尿降低脑脊液形成率[47].在两种先天性[48]和老化[18在CPe中,NKCC1的表达改变与脑脊液形成率降低有关。老年人群中使用的药物,如利尿环药速尿和抑制脉络膜钠的心脏糖苷类药物+泵(49]),降低脑脊液形成率,因此可能加剧高龄对大脑的有害影响。需要研究如何解决顶端膜转运蛋白,以及离子通道的K+, Cl-和HCO3.-[50],可根据具体的临床需要,操纵以增加或减少脑脊液的形成率。
2.3调节运输的酶
在实验环境中,Na+- k+- atp酶和碳酸酐酶是CPe中的两种酶,在脑脊液形成的抑制研究中得到了最广泛的分析。Na+- k+- atp酶,或者Na+非典型地(在上皮细胞中)位于CPe的管腔或脑脊液面。因此乌巴因抑制Na+泵(它是脑脊液形成的组成部分)当静脉内放置时,但不是静脉内放置。除了干扰脑脊液的产生,Na+- k+- atp酶抑制也会改变CPe体积、电位差和离子稳态[51];因此,瓦巴因和其他心脏糖苷在调节人脑脊液形成方面的价值有限。另一方面,乙酰唑胺对c.a.的抑制对CPe功能的影响较小,因此可用于治疗减少CSF的产生。由于多种ca亚型在脑脊液中表达,因此在血- csf界面可能存在多种调节流体动力学的靶点。
c.a.群中普遍存在的酶将细胞酸碱现象与脑脊液的形成结合起来[52].减少脑脊液形成的一种最早但仍在临床上有用的方法是减少细胞内不稳定离子(如质子和碳酸氢盐)的产生,这些不稳定离子为CPe面向等离子体和面向脑脊液的两极的流体转运体提供营养。胞质c.a. II催化CO的细胞水合作用2产生H+和HCO3.-。乙酰唑胺,一种磺胺类药物,可以减缓这种反应[44].因此,这提高了脉络膜细胞的pH值,从而降低了H+基底外侧钠的可用性+- h+交换(43,53,54].c.a.的膜结合异构体(例如,c.a. VIII)可能接近于基底外侧HCO3.-向其提供HCO的转运体(如阴离子交换剂2或AE2)3.-与间质Cl交换-[55].寻找非磺胺类药物来选择性抑制特定的c.a.s异构体,II, VIII和XII是值得的[56- - - - - -58].确定针对某一特定攻击线的药物[59可能有助于减少慢性乙酰唑胺给药引起的全身副作用。
乙酰唑胺通过降低c.a.a活性来破坏细胞酸碱平衡,为转运蛋白和水通道蛋白的功能提供了推断性的见解。CPe pH值我急性暴露于乙酰唑胺(1小时)后pH值增加0.3 - 0.4个单位[43,53].长期服用乙酰唑胺可显著改变CP功能和结构[60],包括含有AQP1通道的顶端微绒毛。在肾脏和睾丸(另一屏障组织)中,乙酰唑胺下调AQP1的表达[61- - - - - -64],可能通过pH值的方式我改变。对于肾脏中的液体转移,钠的重要性至关重要+- h+反端口交换(通过NHE3)和pH我在nhe3敲除分析中揭示了维持AQP2和NKCC2系统完整的稳定性[39].在生理上类似的CPe中,多个转运体系统(NHE1和NKCC1)与AQP1通道功能的协调,显然允许CPe离子和体积稳态与CSF分泌同时发生[38].
2.4水通道或水渠
另一种调节脑脊液形成的潜在途径是利用脑脊液中水通道蛋白(AQP)的表达可塑性[65,66].水通道蛋白通道,促进水在血- csf界面的扩散[67- - - - - -69],出现在发育中的CPe [70,71并在一生中保留下来。AQP1,最初指定为CHIP28 [72],在CPe面向脑室的膜上大量表达[73,74而不是血脑屏障(BBB)内皮。因此通过AQP1的调控磷酸化或泛素化[75],有可能选择性地调节从血液进入脑室的水的运动[76].在AQP-1缺失小鼠中,脑脊液形成能力显著降低;因此,csp的相应降低[77,78].这些敲除研究表明,CPe顶膜中AQP1通道的数量对脑脊液制造能力有重要影响。
大自然进行了一个AQP1在晚年缺乏的实验,这对脑脊液动力学有重要意义[57].因此,老年(20月龄)Sprague-Dawley大鼠CPe中AQP1的表达明显低于年轻成年大鼠[57].因此,衰老大鼠形成脑脊液的能力较差[79].人类CPe表达AQP1 [80].当脑脊液周转率受到AD和NPH的损害时,这增加了在治疗上上调或恢复AQP1表达的可能性[3.,19].相反,在先天性脑积水中,可下调CPe中AQP1的表达或通道活性,从而通过抑制脑脊液形成率来降低ccsf [77,78].心房利钠肽(ANP)是一种csf调节剂,被认为是AQP1通道功能的调节剂[69].
2.5神经肽受体
脑脊液中的神经肽刺激脑脊液中的多肽能受体改变第二信使的代谢和与液体形成相关的离子转运[j]。81].脉络膜精氨酸抗利尿素(AVP)在功能上与多种体液调节肽相互作用(表1)3.).血管紧张素(Ang II)和碱性成纤维细胞生长因子(FGF2)可促进CP中AVP的自分泌抑制调节。在刺激下,ANP和AVP的脉络膜受体都能诱导深色上皮细胞[82,83]在体外以及在活的有机体内。暗CPe细胞具有神经内分泌作用,可下调脑脊液的产生。V1抗利尿激素能受体刺激诱导暗细胞[j]83],还原Cl-CPe射流[83],减少脑脊液的形成[84].此外,三种利钠受体的ANP转录本[85]产生环磷酸鸟苷(cGMP) [86]在完整和培养的脑脊液中均表达。在某些生理条件下,ANP抑制脑脊液的形成[87].这种抑制可能是由CPe暗细胞介导的[82在脑积水中更为常见。
当脑脊液动力学不平衡时,对水调节神经肽的脉络膜受体的大量可塑性也支持这一流体稳态模型。脑积水中ANP的CP受体密度有上调或下调的趋势[88],这取决于病理生理(高岭土诱导的和先天性的)。脑脊液神经内分泌调节也反映在空间飞行中脑脊液流体动力学改变或流体转移引起的ANP受体密度变化中[89].此外,AD中AVP的脉络膜结合位点更多[90],一种伴有心室肿大的疾病[3.]和脑脊液压力升高[91].ANP和AVP的肽类似物[17可能证明通过作用于CP神经肽受体来治疗性地调节CSF参数是有益的。
3脑脊液压力
当脑脊液形成和引流明显不平衡时,ccsf或ICP迅速升高。增强ICP减少脑血流量(CBF)和氧合,并在分子水平上可能改变神经元和胶质细胞中的蛋白质表达。因此,由于颅内压升高对脑功能的潜在破坏性影响,评估调节脑脊液压力的因素并设计更有效的监测和治疗扭曲颅内压的方法在临床上具有重要意义。
3.1伺服机制调节假说
ICP是流体动力学和血流动力学参数的复杂函数。两者结合在一起,在成人中产生100-200毫米小时的cfp2通过腰椎穿刺在侧卧位测量O。该压力与CSF产率和流出阻力成正比,通常为70 mm H20 /ml/min及以上th比年轻人多十年[92].
在流体力学方面,反馈下调CSF形成可以降低CSF fp。通过体内平衡调节来减少脑脊液的输出是至关重要的,因为持续的脑脊液浓度升高会损害对中枢神经系统的血管供应[93].因此,阐明神经内分泌液的调节对开发治疗CSFP的药物至关重要。构建ccsf调控模型的一个关键观察结果是,大多数神经肽(包括ANP)的CSF浓度取决于中枢(CNS)来源,而不是外周(血浆)来源[94].此外,脑室内给药ANP可降低因缺血而升高的CSFP [95]或先天性脑积水[96].这些发现促使人们寻找各种组成中枢稳态系统来调节CSFP的元素。
越来越多的证据支持心室伺服机制稳定CSFP。一种假说认为csf -心室周围联系中的压力敏感调节元件通过合成/释放针对CP的肽来做出反应[97].急性调节cspp的主要候选神经肽是ANP。集体实验和临床证据表明:i)脑脊液ANP滴度随脑脊液fp升高成比例增加[98], ii)高压脑积水患者脑脊液中ANP水平升高[99,One hundred.], iii) CP中的ANP受体经历Vmax调节,以补偿脑积水中csp的增加[88,101];及iv) CPe对ANP有生物反应[82]并调节脑脊液的形成[102]通过cgmp依赖机制[86,103].ANP和AVP对CP-CSF的调节作用在急性高压脑积水中出现,但在慢性NPH中明显没有[104].有趣的是,未成熟大鼠(脑脊液相对较低,脑脊液分泌不完全发达)的脑脊液[33])对ANP和AVP调节的敏感性低于成人上皮[83].这可能是由于婴儿与成人在神经肽受体密度和CPe代谢偶联方面的差异。
3.2脑脊液压力产生的个体发生
在啮齿类动物发育过程中,脑脊液的增加与脑脊液形成的早期阶段具有暂时性的相关性。戊巴比酮麻醉的体外胎鼠(18-21天)脑脊液压力约为20 mm H2O,上升至34毫米高20在出生后10天及以后[105].大鼠出生后1 ~ 3周是CP-CSF分泌成熟的分水岭[33,106].因此,出生后早期神经丛血管和动脉灌注的增加[107- - - - - -109]促进CPe逐渐增加的酶和运输能力[110,111].增强的血液流动和代谢率结合起来加速Na+和Cl-进入心室的转运[112].CP的产液增量[113使CSFP升高到成人的水平[105].脑脊液的动脉搏动随着液体周转的增加建立了脑脊液沿神经轴向下移动的压头[114并打开蛛网膜下腔进行再吸收。这种增加的脑脊液分泌和压力脉冲的血流动力学-流体动力学产生促进了脑生长的突增[106- - - - - -113].在发育中的中枢神经系统中维持适当的脑脊液至关重要地取决于导水管通畅和脑脊液流动的顺畅。正如眼压重要地塑造了发育中的眼睛的形状一样,cspp在围产期的典型适度上升[105]有助于改变正在扩张的中枢神经系统。
3.3先天性脑积水和脑室周围区域
然而,对大脑发育的不利影响是由于继发于Sylvian输水管道阻塞的ccsf异常升高造成的。导水管受损的脑积水(H-Tx)大鼠的CSFP增强,在出生后10至21天增加2倍[115].在其他H- tx研究中,CSFP从约20 mm H开始增加20在出生后10天可高达90毫米H20至3周[116,117].血压升高反映出侧脑室外血流阻塞。脑积水导致的脑脊液淤滞干扰了脑和脑室系统的发育[118,119].
缺乏室管膜特异性表达的转基因小鼠[120],促进睫状体功能,在脑室和邻近大脑的解剖关系中有严重的扭曲。某些脑积水畸形源于CP发育过程中的代谢、运输和纤毛缺陷[121].系统的研究应探讨脉络膜-室管膜衬里的纤毛发育缺陷如何影响脑脊液的形成、组成、体积并最终影响脑脊液。
CSFP影响心室周围蛋白的表达和向心室的分泌。最佳生长的中枢神经系统依赖于脑脊液中微妙平衡的生物物理和生化现象[6].然而,在先天性脑积水中,不仅压力增加,脑脊液成分也发生改变[118,119,121].先天性脑积水患儿脑脊液中神经生长因子浓度升高[j]122],但细胞因子水平明显稳定(暗示血脑屏障功能完好)[123].而脑脊液成分的一些改变是由于脑脊液流动中断[119,121],其他成分的变化与压力引起的心室附近细胞氧化损伤的副产物有关[124].脑积水患者脑脊液化学的其他改变,可能是稳态的,可能是由于压力诱导CPe、室管膜和脑室周围组织分泌的蛋白质上调。一个例子是脉络膜生长因子合成对缺血后ccsf增强的反应[7或创伤。CPe和室管膜是生长因子的丰富来源[125,126]修复因cfp升高而损伤的组织及其继发效应[8].
脑脊液压力和血管系统之间的相互作用,特别是在脑积水发病时,有待系统的研究。有趣的是,自发性高血压大鼠的动脉压升高与脑室增大有关,这是通过影响输水管壁的合下器官(SCO)的分泌来实现的[127].SCO及其相关的Reissner's纤维(RF)分泌成CSF糖蛋白,对于建立正常的脑脊液流向神经轴以进行远端重吸收至关重要。因此,SCO-RF复合物的破坏会导致脑脊液流动效率降低,从而导致脑积水[128,129].上海合作组织的职能受到损害[130]以及CP [121导致脑室增大和脑脊液动力学失衡。这些观察结果表明,脑室周围器官在分泌因子以优化脑脊液流量、体积和压力方面具有重要意义。
3.4脑对脑脊液压力升高的反应
除了对心室周围区的压力影响外,ccsf还通过几种方式对大脑产生全面影响。对脑脊液活性升高的反应大致可分为以下几类:1)脑脊液动力学改变对神经结构和代谢的影响;ii)保护实质的稳态转运界面如何响应脑脊液高血压中神经肽的上调。首先,有明显的氧化变化[131- - - - - -133]在脑积水中反映出受伤的神经元代谢神经递质的方式[134]和髓磷脂[135].尽管超出了本综述的范围,但脑积水中有害的厌氧神经元代谢的话题以前已经被讨论过[136- - - - - -138].关于第二种考虑,即稳态机制,CSF中ANP和AVP浓度的调节性增加来自CSF中csp的升高[98- - - - - -One hundred.,104]明显促进多个区域的血管灌注。尽管ANP上调可能会减少缺血和脑积水时脑脊液的形成,但它确实通过增加脉络膜血流量来支持CPe的活力[139].csf给药ANP和AVP使脑动脉扩张[140,141].ANP-和avp -对蛛网膜下腔出血后内皮素所致脑血管痉挛的影响142].中枢上调ANP的灌注支持作用可抑制水肿[143通过稳定CP和受缺血和ccsf增强威胁的脑血管系统。
在慢性脑积水中,即使ccsf适度增加也会损害CBF和代谢。cfp的间歇性变化需要深入分析,特别是对区域流体动力学和血流动力学的影响。很明显,前瞻性和回顾性研究[91]对于推进脑脊液疾病的治疗策略至关重要(图2)。6).
3.5脑脊液波形测量的进展
ccsf波分析提供了对脑脊液动力学状态的实质性见解,比脑灌注压和平均颅内压的评估更可靠,特别是当基线压存在差异时[144].脑脊液有一个特征性的压力脉冲,随健康和疾病而变化。心血管参数通过影响脉搏幅值和潜伏期的收缩期和舒张期成分显著影响CSFP波[j]。145- - - - - -148].动脉压力脉动通过CPs传递到心室液[114并产生脑脊液压力波。对脑积水有临床应用价值[149来表征脑室-蛛网膜下腔系统的压力波。
颅内压如何记录?传感器放置在脑脊液、脑实质或硬膜外间隙是否重要?用Camino OLM ICP和Codman ICP微传感器等传感器记录了连续的ICP信号[144].一项对脑实质和硬膜外空间监测的研究显示,记录的平均压力有显著差异,但在平均ICP波幅和平均ICP波潜伏期参数上没有差异[150].因此,硬膜外ICP记录(以估计实质压力)对于确定单波脉冲压力幅度(dP)和单波潜伏期(dT,或上升时间)等参数是可行的。此外,监测脑室内的ICP作为波形参数,其结果与用脑实质传感器进行的压力测量结果相当[145].缺乏证据表明实质和脑脊液之间存在明显的压力梯度。
在评估颅内顺应性时,ccsf的脉动成分可能比平均ccsf更有帮助(图2)。7).Eide介绍了一种连续记录100 Hz ICP信号的方法,将其转换为数字数据,然后在6秒的时间窗内进行处理[151].在接受心跳引起的单ICP波进行振幅和延迟分析之前,算法过滤噪声。波幅分析在小儿脑积水中也很有前景[152因为它比平均压力更能预测颅内顺应性。如果术前脑脊液平均波幅> 5mmhg,脑积水或颅缝闭锁所致颅内高压患儿术后预后较好[152].为了确保处理波形的质量控制,算法分析筛选出梗死诱发的波以提高诊断信息[153].
ICP/CSF波形分析对成年慢性脑积水患者的预后具有预测潜力。虽然特发性NPH (iNPH)患者可能有正常的平均ICP,但他们有可能改变了单个ICP波。在分流后最终改善的iNPH患者中,发现其平均ICP波幅值较高[154].在一个队列中,就分流后一年的阳性临床变化而言,平均CSF波幅比CSF流出阻力(Ro)更能预测[155].高达60%的iNPH患者平均脑脊液波幅增加,其中90%的患者对分流反应良好[156].分流后认知结果[157]在术前平均ICP波幅较高的iNPH患者中表现较好(图2)。7).
脑脊液中所谓的B波,特别是在NPH患者中,可以预测成人慢性脑积水手术后的预后。然而,慢B波与分流手术后的改善仅呈弱相关[158].提出了一种替代B波检查的方法。因此,相对脉冲压力系数(RPPC)结合了脉动容积变化和弹性对cspp的影响[159].RPPC反映的是脑脊液的再分配/储存,而不是再吸收,因为它将脉冲振幅与平均脑脊液fp联系起来。
一个有价值的临床目标是用对脑脊液或大脑干扰最小的方法来确定绝对的脑脊液fp。脑脊液与耳、鼻、眼的液体相邻。例如,轨道血管系统暴露于环境cfp中。这应该能够通过超声和动力测量数据可靠地测定CSFP。基于眼动脉(血流)和静脉(流出压)测量的经验指数与绝对CSFP高度相关(r = 0.95) [160].因此,这种有前途的间接目测方法值得改进。
直接测量的CSFP也取得了技术进步。一种新的技术,最大限度地减少中枢神经系统的侵犯利用空心管。这种脑室探头可以精确地插管脑脊液并确定脑脊液是否开放,而不会沿穿透导管丢失液体[161].这种改良的mandrin入路只需一次穿刺即可进入脑室,而在以前的插管手术中,偶尔会有多次穿刺来定位脑脊液[161].总的来说,CSFP评估的目的是通过最小程度地干扰csf -脑来实现可靠性。
为了加快脑脊液和脑积水的建模,我们正致力于描绘脑脊液信号。高精度的血流动力学和流体动力学参数信号有助于CSFP分析。连续信号输入到多个传感器(输液时的血压和ccsf)通过软件集成[162]来评估流体动力学并预测输液试验的稳态反应。通过分析与搏动血流相关的脑电阻抗变化,计算机化血流成像无创评估NPH [163].通过血流脑电图测定动脉顺应性是通过动脉脉冲振幅(aAMP)对平均ccsf的回归来评估的。动脉顺应性较低的患者aAMP与CSFP的斜率值较高。越来越复杂的ccsf对动脉压的分析将改善预测分流。预测心室内压力和流量的流固相互作用模型[j]164]和向脑实质传递压力[165,166]正在推进脉动流体动力学理论。
4脑脊液流量
脑脊液流动途径需要阐明健康和患病的大脑。脉络膜分泌的脑脊液沿着神经轴流向4th脑室,然后通过后脑孔进入基底区的大池和蛛网膜下腔。除了这一经典描述的途径外,新的证据表明脑脊液也通过另一途径流向基底池和中脑池,即进入蛛网膜下腔延伸[167[间膜的](源自背侧的理查德·道金斯脑室)和上髓膜(吻侧4th心室)。脑脊液从大池流向皮质蛛网膜下腔区和蛛网膜绒毛的有限性需要进一步评估[168],脑脊液大流量在脑室和损伤/水肿脑实质之间可能分流[169].对脑脊液分布路线的了解将有利于药物治疗方案。
4.1脑脊液流量与脑代谢
越来越多的人认识到脑脊液流量减少会对脑代谢和体液平衡产生不利影响[3.,18,19,118,119].历史上在脑积水调查中,脑脊液压力和体积[170- - - - - -173],而不是流动和成分,在动物模型和分流设计中被强调。因此,在脑室-蛛网膜下腔系统的压力-体积关系方面积累了相当多的知识。然而,越来越多的证据表明脑脊液流动对脑代谢的重要性。由于CP-CSF为神经网络提供微量营养素和多肽,并清除许多分解代谢物,因此脑脊液流动受阻会扰乱生命早期的代谢[119]以及在后期[174].
4.2流动对胎胚基质的影响
胎儿期脑脊液经脑室和导水管的流动受到干扰会严重延缓大脑发育[j]。118,119].这部分是由于生长因子从分泌部位(如CP)转运到心室下萌发区(干细胞成为神经元的地方)受到损害。H-Tx型脑积水大鼠存在先天性缺陷,导致输水管区组织发育不良[175,176].H-Tx模型[117- - - - - -119]显示出产前脑室肿大,甚至在脑室内压力升高之前,脑脊液生长因子通过体积传递传递的扭曲。因此,由于神经前体细胞的错误分化,产前改变的脑脊液流量导致H-Tx发育不良[118].因为CP功能是中枢神经系统发育的基础[2],评估脑脊液流动和成分紊乱如何损害正在发育的大脑是相关的。导水管脑脊液流量无创定量分析[j]177]将提高对儿童脑积水的认识。
4.3老化中枢神经系统CSF流量减少
成人慢性脑积水的脑脊液血流中断也会破坏大脑功能。随着年龄的增长,CP上皮制造脑脊液的能力不断下降[2,3.,57,79].由于脑脊液的形成率在衰老和疾病中减少了50%或更多[3.,19],下沉作用[33慢流脑脊液被减弱[9].脑脊液中潜在毒性肽和有机代谢物的浓度[174大脑因此会因为流动迟缓而建立起来。分解代谢物从ISF扩散到脑脊液的浓度梯度较差,导致大脑对有害物质的清除减少。老年动物血流抑制剂(如乙酰唑胺)的药理研究[36,53], fgf2 [178,179]和高岭土[180]来分析急性和慢性血流减少状态下脑脊液蛋白浓度升高的时间过程。
4.4改进无创流量测量
由于先前的技术限制,在动物模型中评估脑脊液流量的研究一直很缺乏。然而,一些涉及磁共振成像(MRI)来量化脑脊液流量的非侵入性研究已经在人类中进行了。Ridgway等人最早的分析之一。[181]表明脑脊液的流动是搏动的,即在头侧和尾侧交替流动。因此,他们使用MRI脉冲序列(从心电图的r波门控)来计算CSF流速(例如,2.9 cm/秒)和相应的流速(例如,0.4-0.6 ml/min)。类似地,采用多层自旋回波方法对脑室造口术前后的脑脊液流量进行动态MRI比较[182].磁共振相位成像也被用于证明人类脑脊液流量的昼夜变化,后者在夜间是白天的两倍[183].
近年来在无创定量脑脊液流量的技术和算法方面取得了进展。Stoquart-Elsankari说,使用相衬MRI计算心脏周期的CSF和CBF曲线等。[184]提取了几个脑脊液参数的数据:平均和峰值流量、潜伏期和行程体积。他们发现,老年人脑脊液中风量减少,在输水管和颈椎水平都是如此。另一种新的方法是相衬平衡稳态自由进动(PC-bSSFP)。与梯度回波相比,它的优点是提高了信噪比,可以更有效地分析非层流CSF流[185].PC-bSSFP比梯度回波法更适合于定量脑脊液前池和颈蛛网膜下腔的湍流脑脊液流[j]。184,185].将精细的成像程序应用于小动物模型将有助于模拟血流脉动和心内周期脑脊液容积位移。
5脑脊液容积
维持正常的脑脊液容量对大脑健康是必不可少的。脑脊液容量范围从狭缝脑室综合征的空间大大缩小到严重脑积水的脑室肿大。脑室收缩和扩张的动力学尚不清楚,但可能涉及三个主要因素的相互作用:脑组织特性的变化(如顺应性)、脑脊液动力学和血管参数。脑脊液容量可显著改变医源性的次优率脑脊液通过分流。血脑屏障和BCSFB破裂的疾病也会改变心室容积。由于脑代谢和血流的变化对神经元功能的影响,了解脑脊液体积是很重要的。因此,需要关于局部脑脊液容量调整的速度和程度的信息。
维持脑室-脑池-蛛网膜下腔室的适当大小是生物物理和生化复杂的。成年哺乳动物的脑脊液容量从小鼠的0.04毫升左右[77]至约150-160毫升[3.].在生物体的整个生命周期中,脑脊液的体积会随着压力的变化而变化。神经丛灌注不足[186- - - - - -188]打断了O2严重损害BCSFB和心室完整性。高温也破坏了脑室与脑室的联系。通过脑脊液和脑脊液之间的渗透和自主神经破坏,热疗引起中枢神经系统实质水肿性扩张[189].另一方面,心室容积可收缩,如心室裂缝综合征[190].转基因、脑积水和高血压模型揭示了改变心室容积的个体发生、生理和生理因素。下面讨论血管、流体动力和神经内分泌现象在调节脑室大小中的重叠作用。
5.1血流动力学因素
脑脊液容量对脑血容量(CBV)的生理变化有重要的调节作用。因此,脑血管系统内血液量的增加导致脑脊液的位移和体积的减少。相反,CBV的减少可导致CSF容量的增加。根据Munro-Kelly原则,CBV和CSF体积之间或多或少的相互关系反映了这样一个事实[191],血液、脑脊液和脑的总容量在以刚性颅骨为界的颅内空间中保持相对恒定。因此,为了调节中枢神经系统内的压力,脑脊液是一个有用的物理缓冲,有助于适应脑供血的变化。
脉络膜血流动力学的物理方面也显著影响脑脊液体积。神经丛有3-4毫升/克/分钟的轻快、搏动的血流[108,109].强烈的动脉脉冲穿过脉络膜上皮膜到达脑脊液。因此几乎所有的脑脊液运动都是搏动的。人们早就知道脑脊液动力学受到脑脊液血管压力波的显著影响[114].当脑脊液脉冲在脑脊液中流动的阻抗增加时,高动力上游CP脉冲使脑室扩张[192].随着下游脑脊液阻抗的升高,脑脊液脉冲从蛛网膜下腔室重新分布回心室和毛细血管-静脉循环。Egnor及其同事提出脑积水与脑室肿大的沟通是由颅腔内的脉冲重新分布引起的[192].
5.2水动力因素
脑脊液分泌减少,可能是由于SLC4基因敲除小鼠脑脊液中碳酸氢盐运输中断而导致的,从而大大减少了心室容积[193].另一方面,主动代谢的脑脊液乳头瘤的脑脊液分泌增多[194],容易导致心室扩张。因此,脉络膜血-脑脊液界面运输和通透性的改变显著影响心室容积。
自发性高血压大鼠模型(SHR)也揭示了BCSFB转运和液体形成在调节中枢神经系统内部液体量中的重要意义。SHR显示心室肿大[127,195这可能是由于CP功能的显著转变。与非高血压Wistar-Kyoto (WKY)对照相比,离子、水和非电解质更容易穿透SHR的血- csf屏障[196].SHR大鼠的CPe始终具有更多的线粒体数量,高尔基体加工增加和运输活性增强[197].SHR中较高的血-CSF界面渗透性允许有机溶质(如蔗糖)从血液渗透到CSF [196].Na活性增加+- k+2氯-转运蛋白(198]促进CP内的流体转移[1],也发生在SHR中。SHR脑脊液的渗透性和分泌量越大,可促进脑室内液体的快速转移。这与SHR的心室扩张一致[127,195].根据Egnor模型[192], SHR中传递动脉脉冲的较大脉冲幅值也可能是导致心室增大的一个因素。
其他血-脑脊液屏障损伤模型揭示了心室容积失调。成年大鼠急性动脉高血压瞬时打开BCSFB,使血浆蛋白渗漏到心室[199].增强脑膜通透性的病理干扰导致大分子在正常低蛋白脑脊液中积聚。这增加了脑脊液的渗透压,并将水引入脑室。短暂性前脑缺血也会破坏脉络膜超微结构和转运蛋白[187],导致脑脊液内稳态暂时丧失。对高血压和缺血性脉络膜循环损伤的进一步分析应阐明修复机制[125恢复CPe和心室容积的稳态。
5.3神经内分泌因素
多肽在BCSFB和BBB处调节的流体转移[j]200,201]分别帮助设定脑脊液和脑ISF的体积和组成。此外,由神经肽介导的室管膜界面液体交换的微调[202]和生长因子[125影响心室和间质间的液体平衡。当转运界面的这些协调的内稳态机制被破坏时,心室可以扩张或收缩。
在CP的血- csf界面,ANP、AVP和FGF2及其顶膜受体之间存在复杂的相互作用,控制离子和水分泌到脑室。这三种多肽通过神经内分泌对CPe的影响下调脑脊液的形成[2,6,17,81- - - - - -87].在CP-CSF系统中ANP、AVP和FGF2水平主要受中央控制[6,98,203- - - - - -208因此在很大程度上不受血浆和外周效应的影响。当中枢神经系统受到生物化学或物理干扰时,这些肽能系统被激活以恢复正常的水合作用和渗透压。通过这些机制,中枢神经系统的细胞外和细胞内液体体积稳定[209].
脑室大小受脑脊液输出的肽调节的影响。FGF2有许多生理作用,但一个新认识的是液体调节。外源性给药FGF2在活的有机体内和在体外减少脑脊液的形成[178,179].脑脊液抑制剂AVP的脉络膜释放明显促进了fgf2诱导的液体生成抑制[210].FGF2和AVP在CPe中的表达,与下丘脑-垂体轴的表达一样,对机体的水分平衡很敏感[208,211].有趣的是,在SHR的增长中,CPe中FGF2水平的持续下降(可能导致脑脊液产生的抑制性减弱)与心室大小的逐渐增加暂时相关[195].有证据表明脉络膜FGF2参与心室容积调节。
ANP也被认为是一种体积调节肽[212].一些研究者报道,心室肥大性SHR大鼠的脉络膜ANP受体下调[103,213- - - - - -216].因此,ANP张力的降低降低了SHR CPe中抑制csf的第二信使cGMP的产生[103].ANP是外周系统细胞外液容量的下载器,在中枢神经系统中可能具有类似的功能。SHR大鼠CP中ANP受体的贫化[j]103,213- - - - - -216]可能导致脑脊液产生的抑制减少,从而降低维持正常心室容量的相关能力。因此,观察到SHR中脑脊液形成的增加[196],可能是由于利钠调节减弱,与心室肿大一致。问题是SHR大鼠ANP(或相关神经内分泌)系统的遗传改变是否排除了脑脊液体积下调。
为了构建CSF-ISF体积稳态的全局模型,需要更多关于ANP、AVP和FGF2如何协同作用来调节CP和BBB之间的流体传递的信息。200,201,209].AVP还与CP-CSF系统中的血管紧张素II相互作用以减少产液[217].中枢神经系统液体重吸收部位的神经肽能调节有待阐明。对不同区域脑脊液流动的多肽能调节的深入了解可能使天然配体或其类似物和拮抗剂的使用成为可能[17以治疗性地纠正异常的心室大小。
6 CSF周转率
大脑转换或更新脑脊液的能力对于维持中枢神经系统的代谢平衡至关重要。这是因为大脑缺乏淋巴毛细血管。因此,它在很大程度上依赖连续的脑脊液对流来清除神经元环境中的大分子和分解代谢物。这种清除缺陷,如在脑脊液停滞状态下,当周转率严重受损时,会导致间质、血管壁和脑膜组成的灾难性变化。因此,神经元受到损伤。稳定老化中枢神经系统的药物治疗策略可能包括维持脑脊液形成和防止心室增大的方法。
脑脊液周转率定义为24小时内产生的脑脊液体积除以脑脊液空间的体积。在年轻成年大鼠中,脑脊液总容量每天更新约11次,而对照组为4次/天(表1)4).此外,在啮齿动物和人类中,脑脊液的周转率随着年龄和痴呆的进展而下降(表1)4).脑脊液周转率的下降部分是由于脑脊液在生命后期形成脑脊液的能力下降[18,79].
6.1心室肿大的不良反应
换手率的另一个重要因素是脑脊液的体积。在年轻人中,脑脊液空间为150-160 ml,形成速率约为0.4 ml/min [3.].结果是人的正常周转率约为每24小时4卷脑脊液(表1)4).然而,在衰老和痴呆时,脑脊液的体积或空间增加,通常作为一种疾病真空交货脑积水继发于脑块萎缩性丧失。大脑室固有地损害了脑脊液有效自我更新的能力,因为周转率与脑脊液体积(脑室、贮液池和蛛网膜下腔)成反比。因此,在衰老过程中,NPH和AD(表1)4),脑脊液周转率可下降3 - 4倍。因此,随着脑室在衰老和疾病中增大[3.]时,脑脊液的纯度逐渐丧失,因为其转换速度较慢,导致细胞外液停滞。
6.2减弱的脑脊液汇作用
无论是年轻还是年老的中枢神经系统,脑脊液紊乱通常都涉及液体转换不足。脑脊液吸收去除分解代谢物的作用是流体形成和脑脊液体积相对于脑容量的函数。围产期BCSFB运输能力较弱时,CP每质量组织形成液体的速度比成人慢[33,106,107,110- - - - - -113].此外,在生命早期,CP-CSF体积与脑体积的比例相对较高[34].这些因素降低了未成熟大脑消除不需要的分解代谢物的能力。生长的合成代谢脑需要一个最佳功能的CP-CSF来去除分解代谢物以及提供微量营养素。先天性脑积水,随着脑室的扩大,进一步降低了胎儿本来就很低的脑脊液下沉作用[33,113].因此,婴儿脑积水时脑脊液的低周转使得成熟的中枢神经系统特别容易受到损伤。
在以后的生活中,脑脊液的周转率也明显降低[2,3.,9,18,19,79].在衰老、NPH和AD时,脑脊液形成率逐渐降低,心室容积增大。这三种状态的净结果是脑脊液周转率降低(表1)4).这种减弱的脑脊液汇在衰老、NPH和AD中的作用[3.,19改变脑脊液成分(见下文),对大脑造成有害后果。在衰老过程中,当液体渗漏和间质沉积减少阻碍脑溶质的清除时,神经递质代谢物(如同香草酸)从间质到脑室的通量减少[218可能反映了ISF和CSF之间的血流和扩散减少。在模拟NPH的大鼠模型中[219],与NPH患者一样,β淀粉样肽(Aβ)在中心积聚。在这两种情况下,Aβ清除途径受损(图2)。8),通过减少血脑屏障处低密度亲脂蛋白受体相关蛋白(LRP-1)的转运[219]和减弱的脑脊液动力学导致的体积流量减慢[3.,79].药物干预[11,12,15- - - - - -17老年患者维持脑脊液形成和最小化心室扩张可能防止脑脊液周转减少。一个有价值的目标是提供营养药物或CP移植[12,15通过稳定脑脊液容量和内容来减少神经退行性变。
7 CSF成分
从历史上看,脑脊液成分分析已被广泛用于监测脑代谢扭曲,评估屏障运输和通透功能的破坏,获得靶向脑实质药物的药代动力学参数,以及识别有助于中枢神经系统疾病诊断和预后的生物标志物。因此,脑脊液包含有价值的生化和细胞信息,可以有利于更有效的临床管理脑并发症。对脑脊液成分变化的认识,特别是与血浆相应变化的关系,在解释科学和神经学数据方面特别有用。
7.1 CP-CSF系统的肾样作用
大脑在很大程度上取决于脑脊液成分的稳定性[220],类似于人体依赖于稳定在可承受范围内的等离子体化学。就像中枢神经系统内的肾脏一样[34], CP在动态调节脑细胞外液中起着重要作用[1,18,27].脑脊液成分受到脑脊液上皮中一系列复杂转运蛋白的精细调控[1,18,46,68,220,221].脑脊液离子和肽浓度的严重偏差需要恢复正常[17].当脑脊液内稳态失效时,神经元功能变得脆弱[18,19,222].一个主要的翻译挑战是在CP和血脑屏障运输能力减弱的情况下,纠正衰老、NPH和AD中脑脊液溶质扭曲[3.,9,18,79,219,223].脑脊液成分的稳定很大程度上取决于屏障转运蛋白的药理学操作和受损的BCSFB或BBB的恢复。223- - - - - -225].为了帮助控制某些脑脊液疾病,蛋白质的异常浓度[226]和分解物[174]需要对NPH和AD的不同阶段进行分析和分类。
7.2衰老和疾病时脑脊液生化改变
脑脊液的生化分析在诊断和预后方面具有巨大的潜力[227].在疾病状态下,脑脊液成分被入侵的免疫细胞、血浆细胞因子和病原体所改变[5];因此,脑脊液在临床上可用于评估:1)脑积水或痴呆患者的大脑营养和营养状况[228];ii)中心阴离子和肽重吸收系统对衰老和AD的净化能力[229], iii)针对神经元或脑膜的某些csf载剂的治疗或细胞毒性浓度[230],以及iv)异常溶质的存在[231]或非典型浓度的正常分子。溶质浓度曲线可以确定某些疾病状态,并用于评估治疗干预的益处。
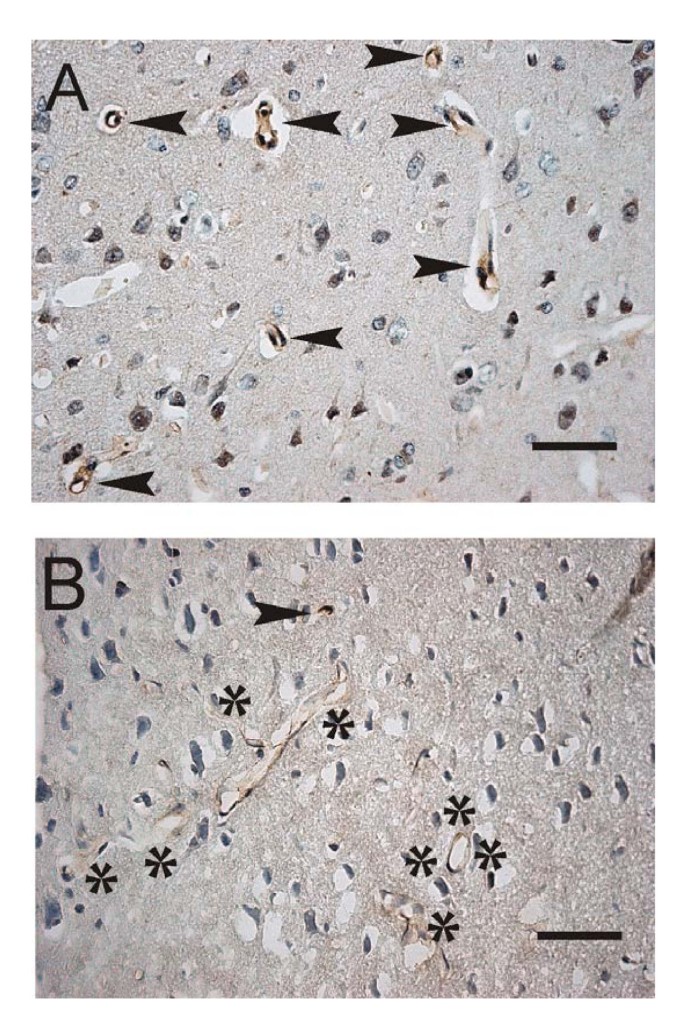
为了维持大脑,脑脊液提供了维生素、多肽、核苷和生长因子的完整补充[1,2,10,27,222,232].通过脑脊液对神经元的充足营养支持在衰老过程中受到损害[79].这可能是由于饮食缺乏加上低效率的CP-CSF运输机制减少了微量营养素向大脑的输送[18,57,223].维生素B和C通过脑脊液转运到脑脊液和邻近的神经组织[222- - - - - -234].随着年龄的增长,CP大量间质纤维化(图2)。9)和对上皮的氧化损伤[223破坏了这条重要的运输路线。结构和生化破坏不仅会降低脑脊液的形成速度,还会降低AD患者脑脊液中有机物的分泌[228].总的来说,老年人的脑脊液浓度数据应根据血流减少和代谢改变来解释[218].
脑脊液中的蛋白质也会在晚年变得缺乏。转甲状腺素(TTR)由脑脊液广泛合成并分泌到脑脊液中。TTR是一种有用的脑脊液标志物,因为它主要由脑脊液[235]如果有的话,只有轻微的脑实质[236].TTR的一个功能是结合a β,从而使其稳定在可溶性形式并防止中枢神经系统肽毒性[223这可能发生在Aβ自组装成神经毒性低聚物时。老年和AD患者脑脊液中TTR水平降低[j]237,238].脑脊液缺乏TTR可能使脑间质易发生Aβ寡聚物毒性和斑块形成[j]。223].需要一些策略来维持老年人CP的TTR分泌,例如通过尼古丁调节[239].此外,CP分泌的一系列生长因子有助于修复前脑缺血或神经退行性损伤[7,17,125,126].大脑健康需要持续的脉络膜分泌肽和蛋白质的混合物,以影响脑脊液和神经元-神经胶质网络的平衡代谢稳态。
除了接收脑脊液的生产性分泌物外,脑脊液也是脑外扩散的分解代谢物的储存库。过量的代谢物从脑室流出可使脑脊液中毒。脑脊液中由过氧化现象产生的有毒分解代谢物随着年龄和神经退行性变而增加[174].AD患者脑脊液糖化蛋白升高[j]231].保护和滋养csf -脑联系的CP组织在老年和AD中遭受氧化损伤和代谢中断[18,223,240,241].当有毒的神经元产物(如Aβ)从大脑进入脑脊液并对已经因衰老而衰弱的CP造成进一步伤害时,恶性循环就随之而来了[57,79].脑脊液上皮中Aβ的稳定积累可能干扰瘦素从血液到脑脊液的运输[242].BCSFB转运的改变可能通过干扰经脑脊液向下丘脑的激素信号传递而扰乱神经内分泌平衡。
7.3清关运输的重要性
维持ISF和CSF成分的纯度至关重要,并依赖于有效的清除机制。由于中枢神经系统缺乏淋巴毛细血管,csf介导的代谢物和毒素的清除对于有效的神经元功能是必不可少的。近端和远端CP-CSF系统在清除有害物质方面起主要作用。这发生在三种情况下。首先,脑脊液上皮顶膜上的重吸收转运蛋白主动清除脑脊液中的有机阴离子和多肽[1,17,243].这种脉络膜清除补充了不需要的代谢物从ISF到脑毛细血管的主动重吸收[229];对于给定的分解代谢物,血脑屏障与BCSFB的比例清除率[244[在健康和特定疾病方面都应确定]。其次,不断加工的新生脑脊液流经大脑内部,作为代谢物的水槽,沿着浓度梯度扩散到脑室[1- - - - - -3.,33].这些物质通过脑室-蛛网膜下腔系统大量流至远端引流部位[1,18].毒素清除的第三个方面是通过蛛网膜-淋巴-静脉界面的脑脊液向外流动向下游挤压代谢物[1,7,245].在健康的脑脊液中,这三种处理机制协同工作以影响流体稳态。因此,在脑脊液转换减少的慢性脑积水(NPH)中[3.,19],扭曲的脑脊液化学可以通过加强脑脊液的形成、流动和引流来纠正。代谢物清除缺陷和毒性必须与NPH中已知的缺血性损伤一起考虑,以获得慢性脑积水的完整图像。
综合分析脑脊液生化有助于控制NPH、AD等衰老并发症。几种动物模型表明神经肽和生长因子对脑脊液形成和重吸收有抑制作用[j]。178,246].一个合乎逻辑的延伸是系统地分析人脑脊液在慢性脑积水伴和不伴神经退行性变阶段的生物化学。老年患者脑脊液中蛋白质、多肽和有机代谢物(如鞘磷脂衍生物)的脑脊液谱分析可能有助于了解屏障失效和脑代谢如何与脑脊液动力学缺陷联系在一起。脑脊液白蛋白、神经肽Y、血管活性肠肽和硫脂(皮质下动脉硬化性脑病的缺血标志物)水平升高对分流手术结果有负面影响[247,248].进行性脑内ph和导水管狭窄患者脑脊液成分的系统分析[j]247可能会提高分流效益的预测能力。
7.4成分的治疗性操作
脑脊液和脑ISF成分的药理学操作可能是可行的。一个目标是通过将药物通过BCSFB输送到大脑内部来改善脑脊液的流量和含量[16,17].脑室周围区域(如室下区、海马体和白质)因cspp升高而受损,需要使用修复剂[91],缺血[7,126,186,187和扭曲的脑脊液化学。另一个迫切需要是为脑液周转严重受损的老年患者开发脑脊液清洗程序。这类似于肾衰竭患者的肾透析。脑脊液透析或低流量分流的新技术,特别是痴呆患者亚组,可能改善认知。因此,新药的使用[16]及生物科技装置[15]值得考虑,以减缓退化或促进愈合NPH/AD。CPs和心室[16,17]有望成为获得所需药物浓度和优化CSF组成的调控位点[249].
CSF循环与ISF动力学的关系
CSF和ISF之间的功能相互作用是丰富的。脑脊液和ISF以大流量移动,前者通过大腔,后者精细地通过神经节内狭窄的弯曲通道,大致沿着有髓纤维束移动。流体对流进出脑实质,取决于普遍的局部静水压力梯度。对于微量营养素和多肽向神经元和神经胶质的传递、激素信号向靶细胞的传递、药物向受体的传递以及中枢神经系统中分解代谢产物的清除,了解大流量通路是非常重要的。当ISF和CSF不能自由渗透时,就会出现病理后遗症。由于疾病的影响,脑脊液通过间质途径的运动需要进一步分析。
8.1脑间质脑脊液交换
脑脊液和ISF在脑室管膜(内部)和神经胶质(外部)表面动态交换水和溶质[1,27].脑ISF具有明显的循环特征[22].持续的基金周转,即使周转速度较慢[250,251],为神经元维持最佳的微环境。随着年龄的增长,脑毛细血管内皮和脉络膜上皮的主动运输效率降低。因此,ISF和CSF的缓慢周转导致中枢神经系统积累潜在的有害有机酸和多肽。当代谢物在细胞间积累时,神经元在衰老过程中受到损伤[9].
8.2脑内ISF运动的组成
代谢废物通过ISF和CSF清除途径被丢弃。脑ISF将代谢物从神经元和神经胶质转移到排泄部位。ISF有多个输入和输出组件,保持液体混合并输送到排泄位点。ISF体积和流量的输入侧是一种类似csf的液体,可能是由微血管中的星形胶质-内皮复合物分泌的[252].假定血脑屏障产生的液体比CP少得多。ISF的另一个输入是实质代谢产生的水[252].ISF的第三个输入是一小部分SAS液(最初来自CP-ventricular nexus),通过Virchow-Robin血管周围间隙进入皮层[253- - - - - -255,部分是由动脉和小动脉的泵送作用推动的。因此,这种循环的脑脊液可能会回流到心室。
ISF输出至少有两个分量。首先,溶质(例如,Aβ肽)的定量重吸收通量通过lrp -1穿过内皮细胞进入血管腔[229].随着血脑屏障中LRP-1的表达随着年龄的增长而减弱,CP LRP-1转运体可能需要通过在BCSFB中按比例重吸收更多的Aβ来弥补脑毛细血管中清除的缺陷。另一类通过血脑屏障被重吸收的溶质是有机酸/阴离子,它们通过有机阴离子运输系统(OATS)从大脑主动转移到血液中[256].其次,物质从ISF向大腔CSF有大量流动和扩散[22],最终在蛛网膜部位被重新吸收。需要研究来确定分解代谢物清除率的比例,在血脑屏障vs. BCSFB和大流量,如何随着脑病理的进展而变化。脑间隙液体渗滤[251]比脑室-蛛网膜下腔的脑脊液循环慢得多。ISF的大流量及其携带的分解产物有待全面的表征,特别是关于ISF与脑脊液水动力学的相互作用。
8.3 ISF/CSF动力学和淀粉样蛋白保留受损
ISF和CSF的体积传递在衰老和痴呆中显著减弱[3.,9].当液体周转率下降> 50%时,脑分解代谢物就会增加[19].Aβ40就是一个例子,它是由淀粉样前体蛋白的酶切产生的[229].由于流体动力学的恶化,在衰老、NPH和AD期间,Aβ在ISF和血管周围间隙中积累。我们的工作模型是,中枢Aβ清除受到衰老过程中相互作用因素的损害。在小鼠体内9个月时,放射性标记的a - β1-40的外排转运减少[229],可能是由于血脑屏障腔面LRP-1转运减少所致。LRP-1的丢失会导致Aβ从ISF中去除的速度减慢[229],导致Aβ42积聚在皮质微血管中[257].此外,脑脊液形成减弱可减少心室下沉作用[33从ISF中提取(通过直接进入CSF的浓度梯度)Aβ片段和其他肽。衰老的另一个不利结果是Aβ42在CP上皮、室管膜和蛛网膜细胞中的积累[257].这些与csf接壤的界面控制着中枢神经系统隔室之间的流体运动[1].当有有毒的Aβ时,脉络膜-脑膜组织在稳定脑ISF对抗斑块形成方面可能不太有效。
衰老、NPH和AD中运输和流体动力学减少的累积证据,[3.,19]指出退化的BCSFB中常见的漏洞[18]和BBB [224].高岭土注射液致老年大鼠脑积水引起中枢神经系统多个区域Aβ滞留[j]219].脑蛋白病变的统一模型应该将肽/蛋白质分布动力学与液体周转能力联系起来。ISF功能的完整性依赖于高效的CP-CSF系统和健康的脑微血管。随着老年转运蛋白的分解,脑间质会积累分解代谢物碎片,包括肽碎片。这倾向于浓度依赖的Aβ自组装成低聚物,纤维形成和斑块沉积。需要关于Aβ保留如何改变CBF、动脉肌动蛋白的信息[258], ISF的水力传导性,细胞外通道的扭曲度和基质的粘弹性。这些因素影响isf -心室流体动力学的相互作用,从而影响分解代谢物向排泄途径的传递。
9脑脊液重吸收
脑脊液进入淋巴和血液的清除涉及多种解剖部位和生理机制。脑脊液重吸收中断是脑积水的常见原因。临床脑积水的最终解决取决于流出部位及其调节的知识。当脑脊液保留在中枢神经系统时,代偿机制稳定ICP [97].除了颅神经流出调节外,脊神经蛛网膜通路也可促进脊髓SAS中脑脊液潴留后的液体流出。此外,当中枢神经系统液体超载时,脑毛细血管可能在高压下耗尽受调节的AQP通道来吸收ISF。提高对多部位液体重吸收的了解将有助于更好地管理CSF和ISF充血。
9.1蛛网膜流出阻力
CSF Ro一直是评价重吸收现象的关键流体动力学参数。在方法学上,脑脊液输注伴随脑脊液fp测量已经为人类和动物产生了充足的Ro数据[259].在啮齿类动物中,先天性脑积水中Ro升高[115,260]和nph样状态[178].脑脊液Ro在NPH患者中增加2 - 3倍[261].琼斯和他的同事在老鼠身上的出色工作[105,262研究表明,在正常脑脊液发育过程中,出生后10 ~ 20天,即上游脑脊液分泌增加时,横流窦对脑脊液的Ro重吸收减少[33,113].然而,在脑积水H-Tx大鼠中,由于输水管道阻塞,出生后Ro(侧脑室)增加[115但不像非脑积水对照组那样在后期发育中减少。最近,Eklund和他的同事[259]综述了脑脊液输注所得Ro数据的重要应用。
9.2蛛网膜绒毛与嗅觉引流途径
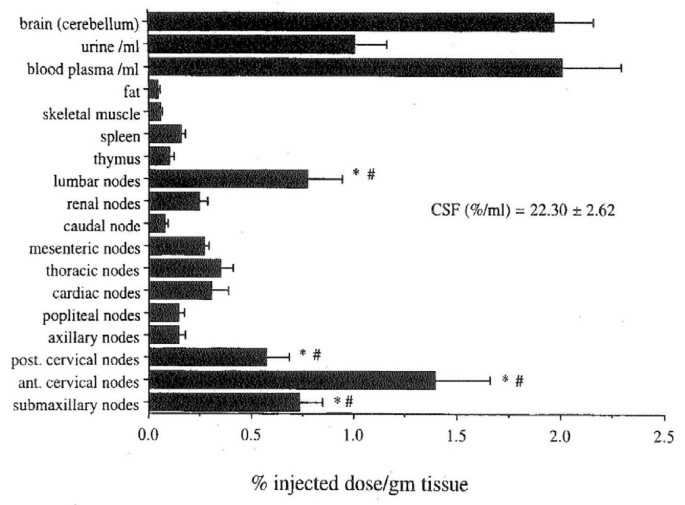
关于脑脊液重吸收的主要部位一直存在激烈的争论。在过去的十年中,在一些动物模型中,脑脊液引流的优势部位逐渐发生了范式转变。因此,脑脊液经嗅觉引流/重吸收[263]和视神经[264]、筛板、鼻黏膜下层和颈淋巴是目前认为从大鼠、猪和羊脑中挤出蛛网膜下腔脑脊液的主要大流量通道[265- - - - - -272];即使是非人类的灵长类动物[269].Johnston及其同事的微膜注射研究提供了大量证据,证明脑脊液流入鼻淋巴是几种物种脑脊液流出的主要途径[266].流行的观点是,在许多哺乳动物中,头盖骨外的淋巴管接受了大量的脑脊液(图2)。10);然而,人类还有待评估在活的有机体内。这种新的强调通过嗅觉途径排水的方法[265- - - - - -272],而不是蛛网膜绒毛,将一个世纪以来关于脑脊液和淋巴在功能上密切相关的观点推向了高潮。
直到最近,脑脊液引流模型强调了嵌入上矢状窦硬脑膜的蛛网膜绒毛的重要作用。每个蛛网膜绒毛被认为具有单向(脑脊液向外)瓣膜样机制,该机制在脑脊液和硬脑膜静脉血之间的正静水压力梯度下打开[252].现在看来,在大多数哺乳动物中,蛛网膜绒毛通常不是大多数脑脊液重吸收的位点,但在脑脊液fp升高的情况下,蛛网膜绒毛可能介导脑脊液清除率的增加[267].在人类中,蛛网膜绒毛在健康脑脊液动态环境中的生理作用有待研究,脑脊液沿脑神经流向眼睛和鼻子的精确机制也有待研究。人脑脊液中的大颗粒[252],与啮齿类动物的细小蛛网膜绒毛相比,表明前者可能在人类脑脊液重吸收中发挥相对更大的作用。
Johnston和他的同事们认为鼻上方的筛状板是脑脊液流出的关键颅外部位。通过筛状和非筛状途径的比例流量评估表明,在低ICP时,脑脊液吸收主要发生在板侧[269].因此,在脑脊液流入鼻粘膜下层和颈淋巴管受阻的情况下,实验密封筛板可用于评估脑脊液流体动力学参数。筛板阻塞大大减少脑脊液间隙,增加颅内压[270并损害补偿脑脊液容量输注的调节系统[269].至少在绵羊中,上述妊娠后期的CSF参数与成人相似[271],包括蛛网膜绒毛相对不受影响与更有功能的嗅觉引流途径[272].Brinker等。[273],在成年大鼠输注期间使用放大x线摄影,早期显示脑脊液通过嗅觉、视神经和颅神经(VII和VIII)进入颈部淋巴。
再吸收的脑脊液最终流入静脉血。因此,静脉闭塞实验提供了特定CSF-静脉界面对CSF重吸收的相对贡献的线索。脑积水(脑脊液潴留)与颅外静脉阻塞受损有关[274].总的来说,这些观察表明嗅觉/颈部淋巴引流,而不是蛛网膜绒毛,是正常脑脊液引流的主要机制[245].此外,当ICP大幅升高时,蛛网膜绒毛和颗粒可作为辅助脑脊液引流途径(通过打开单向阀)。这与早期观察到的静水压力梯度依赖于蛛网膜绒毛的大流量相吻合[252]和高压下蛛网膜上皮内充满液体的囊泡的形成。在沿视神经延伸至淋巴管的薄神经上皮层中观察到孔状开口[275].人类蛛网膜颗粒的有前途的研究在体外(无花果。11),利用室和细胞培养制剂,如由Grzybowski设计的那些等。[276,277],应该阐明流体在静水压敏感孔中的输送。需要回答的关键问题是:蛛网膜细胞孔样结构如何对脑脊液和/或静脉压力升高做出生物物理(超微结构)反应?此外,颅内良性高血压或脑积水如何改变蛛网膜的生化分泌物?颅脑和脊髓CSF重吸收的生物物理和生化数据有待整合。
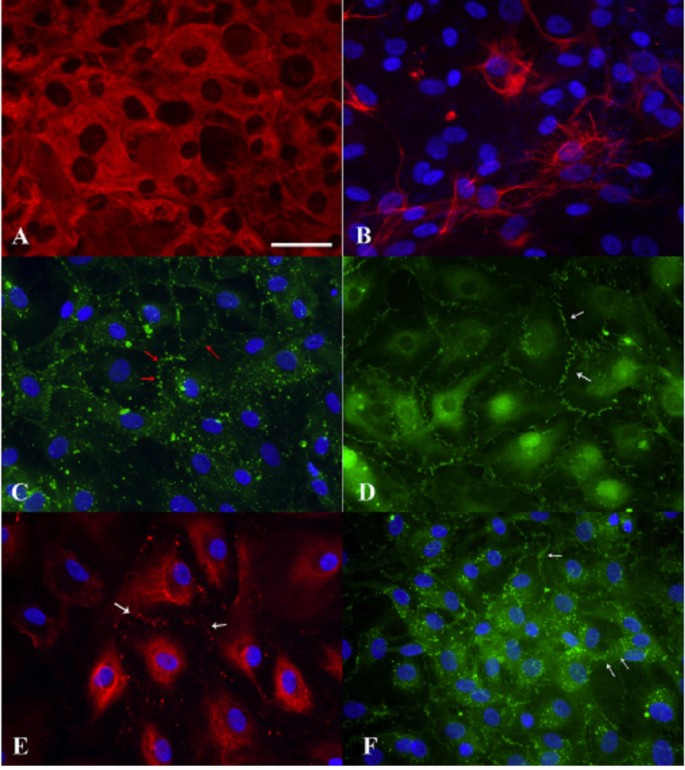
人蛛网膜肉芽上皮细胞骨架蛋白和连接蛋白的免疫染色。A.中间丝蛋白vimentin (Cy3偶联抗vimentin抗体)的表达。B.细胞角蛋白的表达(FITC与广谱抗细胞角蛋白抗体结合)。C. connexin43 (FITC偶联物)的表达;边界处的点状分布(红色箭头)表示细胞培养中的间隙连接。D.细胞-细胞边界(白色箭头)ZO-1(紧密连接)染色(FITC共轭)划定重叠丝状足(平行的短线性结构)。E.桥粒蛋白的表达(Alexa Fluor 555偶联二抗)显示桥粒沿着相邻细胞边界(白色箭头)。F.上皮特异性细胞粘附分子E-cadherin在细胞外围(白色箭头)的表达模式与connexin43和ZO-1相似。所有图像具有相同的尺度(bar = 50 μm)。经霍尔曼许可转载等[277]。
9.3沿脊神经的液体重吸收
脊神经也发生脑脊液重吸收。在一项人体重吸收的脑池造影研究中,向脑脊液注射放射性核素显示,在一小时的测试中,脊髓蛛网膜下腔的放射性降低了20% [278].这种脊髓CSF清除率在体力活动(与休息)的个体中增强。成年大鼠经池内注射高岭土诱导脑积水,脑脊液吸收受阻,沿腰骶椎根有代偿性液体清除[279].在另一项产生大鼠脑积水/脊髓空洞的高岭土研究中,高分子量铁蛋白追踪了从中央管开始的大量脑脊液通道,穿过破裂的室管膜和背柱,然后沿着脊神经进入硬膜外淋巴管[280].这种代偿性脊髓脊液流出可能在直立人类中尤为显著[280].
9.4毛细水通道的重吸收
脑积水影响脑脊液出口并受到脑脊液出口的影响。当Ro升高导致中央液体超载时,可能存在由ICP增强激活的替代非蛛网膜机制,以防止CSF和ISF的进一步积累。血- csf水通道AQPs [78]和血脑界面是调节流体运动的重要控制点。AQPs 1和AQPs 4分别在CP和脑微血管中表达。当颅神经出口、蛛网膜绒毛和脊神经重吸收机制被额外的液体淹没时,AQP表达的代偿性变化可能参与ICP调节。因此,脑积水时(高岭土诱导和H-Tx遗传异常)CSFP升高导致AQP4表达增强[281- - - - - -283].一个关键的问题是,脑积水患者的AQP4上调是否会增强ISF在毛细血管中的重吸收。另一方面,当BCSFB的AQP1下调时,由于脑脊液的形成减少,因此输入中枢神经系统的液体减少,从而降低ICP [77,78].屏障处AQP表达的改变表明,通过与ISF和CSF接触的通道的水通量可以通过药理学调节来修复继发于错误重吸收的脑液失衡。
10建立恢复脑脊液平衡的翻译有效模型
先天性和成人慢性脑积水的体液平衡紊乱的恢复仍然是一个巨大的挑战。由于脑脊液与许多流体隔室和界面复杂地相互作用,因此平移进展是困难的。1).在阐明脑脊液动力学时,不仅需要分析脑脊液-脑脊液-蛛网膜的联系[284还有脑毛细血管- isf -室管膜联系。对高压脑积水(从脑脊液到ISF再到脑毛细血管血)中从脑到脑脊液再到淋巴或相反方向的液体转移的彻底了解,应该加快药物或液体引流设备的治疗。
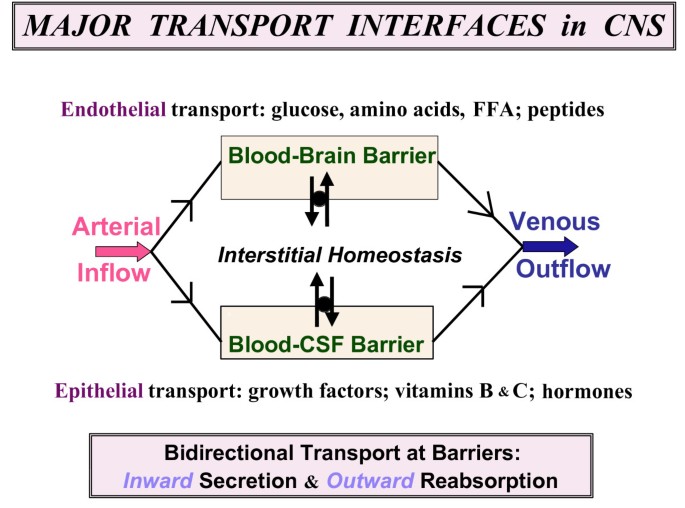
中区警署不仅仅是BBB的附属物[1].相反,复合BCSFB是一个主要的界面,当它与脑毛细血管网络并行工作时(图2)。12),在最佳体积、成分和压力下为神经元提供稳定的细胞外环境。具有稳定中枢神经系统液体的类似肾脏的功能的[34], CP保护大脑,就像肾脏通过稳定血浆成分来保护周围器官一样。为了维持中枢神经系统的稳定,血脑屏障和BCSFB之间是否存在生理上的串扰或信号传导?也许是这样,但要回答这个问题,需要多部门分析。
BCSFB的改变会影响血脑屏障反之亦然。这些主要传输接口上的操作和响应由原位和在活的有机体内允许对障碍进行并发分析的模型在体外细胞培养准备。一种方法是多区隔分析[112]或同时微透析[285脑(实质探针)和脑脊液(池微探针),在全身给予放射性示踪剂后[286].另一种方法是对CP、脑毛细血管、室管膜、神经元和蛛网膜中肽、通道或转运蛋白表达的区域免疫组织化学分析[219].对溶质和水转移的系统分析揭示了流体转移的大小和矢量。此外,分离CP和脑微血管的Western blot、ELISA和PCR数据提供了补充数据[257]描述在活的有机体内传输机制。
脑脊液模型的一个令人着迷的进展是BCSFB和BBB可以参与相反的反应。当中枢神经系统在生理上损害分布途径的疾病中适应改变的水和肽通量(例如,导致Aβ滞留)时,就会发生这种情况。表格5综述了衰老、NPH和AD对血液-中枢神经系统界面水和肽易位的代偿性调节。首先,关于水通过渠道的运动(表1)5),通常情况下,水从血液到大脑的净扩散。然而,在高压脑积水中,ISF中的液体可能通过上调的AQP4通道被净重吸收到毛细血管中。然而,脑积水患者血脑屏障中的这种逆转现象以及AQP1和脑脊液形成的下调,需要从功能上得到证实。此外,在衰老、NPH和AD状态下,通过毛细血管LRP-1从脑ISF到血液的Aβ清除率明显降低,但在重吸收的CSF-CP联系中,LRP-1在这三种状态下上调或维持可能会增加或维持(表1)5 b).这一假设有待动力学实验的证明。尽管如此,越来越多的证据表明BCSFB和血脑屏障在生理和病理状态下是复杂的相互作用。通过整合CP、室管膜、蛛网膜和血脑屏障血管病变的数据,将深入了解CSF-ISF动力学如何影响脑完整性。287].
11的结论
CSF整合了中枢神经系统的多种功能。从胎儿到成年,一直延伸到晚期,CP-CSF积极参与大脑的建设、维持和修复[288].有效的脑脊液稳态机制对神经元网络至关重要。然而,衰老和疾病导致的脑脊液稳态失调会损害运动功能和认知能力。稳定或恢复BCSFB和血脑屏障在衰老和疾病中的功能是下一代研究者的挑战。流体稳态概念的临床翻译取决于接触脑脊液的多种传输界面的扩展知识。
缩写
- aAMP:
-
动脉脉搏振幅
- 一个β:
-
淀粉样蛋白或肽
- 广告:
-
阿尔茨海默病
- AE2:
-
阴离子交换剂,如Cl--HCO3.-逆向转运
- ANP:
-
心房利钠肽
- AQP:
-
水通道蛋白
- AVP:
-
精氨酸加压素
- BBB:
-
血脑屏障
- BCSFB:
-
血-脑脊液屏beplay靠谱障(脉络膜丛)
- :死亡。
-
碳酸酐酶
- CBF:
-
脑血流量
- CBV:
-
脑血容量
- cGMP:
-
环单磷酸胍
- 中枢神经系统:
-
中枢神经系统
- CP:
-
脉络丛
- CPe:
-
脉络丛上皮
- CSF:
-
beplay靠谱
- CSFP:
-
beplay靠谱脑脊液压力
- ELISA:
-
酶联免疫吸附试验
- FGF2:
-
碱性成纤维细胞生长因子
- H-Tx:
-
遗传来源脑积水大鼠脑导水管梗阻模型
- ICP:
-
颅内压
- 安全部队:
-
组织液
- LRP-1:
-
低密度亲脂蛋白受体相关蛋白
- 核磁共振成像:
-
磁共振成像
- NHE1和NHE3:
-
氢钠转化器
- NKCC1:
-
Na-K-Cl共转运蛋白(分泌形式)
- 一组:
-
正常压力脑积水
- PC-bSSFP:
-
相衬平衡稳态自由进动
- Pgp:
-
22运输车
- 愤怒:
-
晚期糖基化终产物受体(Aβ转运蛋白)
- 射频:
-
赖斯纳氏纤维
- 罗依:
-
脑脊液流出阻力
- 该:
-
相对脉冲压力系数
- 情景应用程序:
-
蛛网膜下腔
- 上海合作组织:
-
联合下器官
- 月:
-
自发性高血压大鼠
- SLC4:
-
碳酸氢盐转运蛋白家族的成员
- 竞技场队伍:
-
转体基因。
参考文献
脉络膜丛-脑脊液循环动力学:脑生长、代谢和修复的影响。医学神经科学。编辑:Conn P. 2008, Totowa, New Jersey: The Humana Press。
张建军,张建军,张建军,张建军,张建军,张建军,张建军,张建军,张建军。脉络膜丛-脑脊液系统的发育与衰老。beplay靠谱中国生物医学工程学报,2005,31(1):1-5。
Silverberg GD, Heit G, Huhn S, Jaffe RA, Chang SD, Bronte-Stewart H, Rubenstein E, posin K, Saul TA:阿尔茨海默氏beplay靠谱型痴呆患者脑脊液生成速率降低。神经病学杂志,2001,57:1763-1766。
李春华,李春华。脑膜瘤患者脑脊液动力学分析。神经科杂志(维也纳)。[j] .中国科学:地球科学。
脉络膜丛:全身性疾病的靶点和通往大脑的途径。科学通报,2007,25(6):531 - 531。
张建军,张建军,张建军,等。脑积水疾病对脉络膜丛上皮的生物生理和神经内分泌的影响。神经系统的非神经元细胞:功能和功能障碍。编辑:赫兹L. 2004,阿姆斯特丹:爱思唯尔出版社,31:269-293。
Johanson C, McMillan P, Palm D, Stopa E, Doberstein C, Duncan JA:容量传递介导的脉络膜丛-脑脊液生长因子对前脑缺血损伤的保护作用。血-脊髓和脑屏障在健康和疾病。编辑:Sharma H, Westman J. 2003,圣地亚哥:学术出版社,361-384。
大鼠脑缺血对脉络膜丛的影响。[J]中华血液学杂志,2006,26(6):675-683。
Rubenstein E:脑脊液循环系统衰老与老年痴呆的关系。beplay靠谱中华医学杂志,1998,31(1):283-285。
Emerich DF, Skinner SJ, Borlongan CV, Vasconcellos AV, Thanos CG:脉络膜丛在大脑上升、下降和修复中的作用。生物学报,2005,27:262-274。
Borlongan CV, Skinner SJ, Geaney M, Vasconcellos AV, Elliott RB, Emerich DF:包膜脉络膜丛对亨廷顿病模型的神经保护作用。神经医学杂志,2004,15:2521-2525。
Borlongan CV, Skinner SJ, Geaney M, Vasconcellos AV, Elliott RB, Emerich DF:猪脉络膜丛脑内移植对脑卒中啮齿动物模型的结构和功能保护。中风。2004,35:2206-2210。
Watanabe Y, Matsumoto N, Dezawa M, Itokazu Y, Yoshihara T, Ide C:大鼠脉络膜上皮(修饰室管膜)细胞原代培养的条件培养基对海马神经元神经突生长和存活的影响。神经科学通报,2005,37(3):158-163。
Kimura K, Matsumoto N, Kitada M, Mizoguchi A, Ide C:脉络膜丛室管膜细胞体外促进海马神经元神经突生长。中华神经科杂志,2004,33(3):465-476。
Emerich DF, Thanos CG, Goddard M, Skinner SJ, Geany MS, Bell WJ, Bintz B, Schneider P, Chu Y, Babu RS, Borlongen CV, Boekelheide K, Hall S, Bryant B, Kordower JH:兴奋毒素损伤猴脉络膜丛移植的广泛神经保护作用。中华神经医学杂志,2006,23(3):471-480。
Johanson CE, Duncan JA, Stopa EG, Baird A:脉络膜丛-脑脊液途径药物传递和脑靶向的增强前景。医药杂志,2005,22:1011-1037。
Smith DE, Johanson CE, Keep RF:血- csf屏障中肽和肽类似物转运系统。中国药理学杂志,2004,26(6):565 - 591。
刘建军,刘建军,刘建军,刘建军,刘建军,刘建军,刘建军,刘建军,刘建军,刘建军,等。脉络膜丛上皮与阿尔茨海默病的关系。beplay靠谱脑脊液杂志,2004,1:3-
Silverberg GD, Mayo M, Saul T, Rubenstein E, McGuire D:阿尔茨海默病、常压脑积水和脑脊液循环生理衰老变化的假设。中华神经科杂志,2003,2:506-511。
Milhorat TH:脑脊液生理学。beplay靠谱beplay靠谱脑脊液和脑水肿。1987,纽约:纽约神经科学学会,39-73。
脑间质液分泌和大流量在脑容量调节中的作用。杨建军,刘志强,等。中国农业科学学报,1998,29(5):919 - 920。
脑间质液大流量的证据:生理和病理意义。中国生物医学工程学报,2004,25(5):545-552。
波波M,旋波F:家兔脑室管膜分泌脑脊液。beplay靠谱[J] .中国生物医学工程学报,1997,26(2):344 - 344。
Johanson CE:蛛网膜,蛛网膜下腔脑脊液和神经胶质。血脑屏障导论:方法论和生物学。编辑:Pardridge W. 1998,剑桥,英国:剑桥大学出版社,259-269。
polay M, Stevens FA, Roberts PA:脑室压升高对脉络膜丛血流和脑脊液形成的影响。脑脊液的神经生物学。beplay靠谱编辑:Wood JH。1983,纽约:乌鸦出版社,2:687-695。
Rudick RA, zirtta DK, Herndon RM:小鼠蛛网膜下腔白蛋白清除:脑脊液体积流量的测量。神经科学方法,1982,6:253-259。
脉络膜丛。神经科学百科全书。编辑:阿德尔曼G. 1999,波士顿:Birkhauser, 1: 384-387。
王志强,王志强。脑积水的短期治疗。专家意见,2005,6:1525-1538。
儿童呋塞米的临床药理学:一种补充剂。[J] .中国生物医学工程学报,2001,28(8):779 - 779。
Swetloff A, Ferretti P: E2F5在小鼠和人脉络膜丛上皮细胞内定位的变化。中国生物医学工程学报,2009,29(4):859-865。
Lindeman G, Dagnino L, Gaubatz S, Xu Y, Bronson R, Warren H, Livingston D: E2F-5基因在脉络膜丛功能中的特异性非增殖性作用。基因工程学报,1998,12:1092-1098。
Lindvall M, Owman C:哺乳动物脉络膜丛的自主神经及其对脑脊液形成的影响。beplay靠谱[J]中华血液学杂志,2001,(1):1 - 4。
[14]张建平,张建平,张建平,等。血脑屏障对尿素的通透性及脑脊液对尿素的吸收作用。beplay靠谱[J] .中国生物医学工程学报,2009,32(4):557 - 557。
Spector R, Johanson CE:哺乳动物脉络膜丛。科学学报,1989,26(1):68-74。
沈宏,Ocheltree SM,胡勇,Keep RF, Smith DE:基因敲除PEPT2对头孢地诺酯药代动力学、肾小管重吸收和小鼠脑渗透的影响。中国药品管理杂志,2007,35(5):1299 -1216。
Murphy VA, Johanson CE:酸中毒,乙酰唑胺和阿米洛利:对22Na通过血脑和血- csf屏障转移的影响。中华神经科杂志,2009,32(2):558 - 563。
Murphy VA, Johanson CE:阿米洛利对脉络膜丛钠转运的影响。生物化学学报,1989,(9):187-192。
Murphy VA, Johanson CE:急性代谢性酸中毒和碱中毒患者脉络膜丛和脑脊液中Na(+)-H(+)交换。[J] .中国生物医学工程学报,2009,35(4):557 - 557。
M . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . a . b . a . b。中国生物医学工程学报,2009,35(5):511-522。
李建军,李建军,李建军,等。SCL4A10基因在脉络膜丛上皮细胞基底外侧质膜上的特异性定位。[J] .中国生物医学工程学报,2004,28(2):391 - 391。
Boedtkjer, Praetorius J, Fuchtbauer EM, Aalkjaer C: Na+- hco3 -共转运体NBCn1 (slc4a7)在小鼠中的抗体不依赖定位。[J] .中国生物医学工程学报,2008,29(4):591- 593。
王晓明,李建平,李建平,等。slc4来源的Na+依赖阴离子转运蛋白在人体组织中的表达。[J] .中国生物医学工程学报,2007,31(2):559 - 563。
乙酰唑胺和胰岛素对脉络膜丛上皮细胞[Na+]、pH和体积的影响。[J]中国生物医学工程学报,2009,32(2):557 - 557。
Maren TH: HCO3-合成动力学与液体分泌、pH控制和CO2消除有关。中国生物医学工程学报,1998,35(5):695-717。
王晓明,张建军,张建军。大鼠脉络膜丛钾离子的联合转运。[J] .中国生物医学工程学报,1997,26(2):559 - 561。
Bairamian D, Johanson CE, Parmelee JT, Epstein MH:脉络膜丛中钾与钠和氯的共转运。中华神经科杂志,1997,26(5):523 - 529。
Javaheri S, Wagner KR:布美他尼减少犬脑脊液生产。beplay靠谱中枢神经系统中NaCl共转运的体内证据。中华临床医学杂志,1993,32(2):557 - 561。
Johanson CE, Jones HC, Stopa EG, Ayala C, Duncan JA, McMillan PN:围产期H-Tx大鼠血- csf屏障不同区域Na-K-2 Cl共转运蛋白的表达增强。儿科外科杂志,2002,12(增刊1):S47-49。
张建军,张建军,张建军,张建军,张建军。脉络膜丛Na+/K+活化三磷酸腺苷酶与脑脊液形成的关系。beplay靠谱神经外科,1985,17:768-772。
miller, liu, Bruce J, Brown PD:脉络膜丛离子通道多样性、通道表达和功能。beplay靠谱脑脊液杂志,2007,4:8-
Smith QR, Johanson CE:瓦巴因和钾对脉络膜上皮离子浓度的影响。[J] .中国生物医学工程学报,2009,35(3):394 - 394。
王晓明,王晓明。脑细胞间质液中pH值的变化。神经系统的非神经元细胞:功能和功能障碍。编辑:赫兹L. 2004,阿姆斯特丹:爱思唯尔出版社,31:707-745。
Johanson CE:乙酰唑胺、苯唑胺和全身性酸中毒对脉络丛根尖和基底外膜上氢和碳酸氢盐梯度的不同影响。中华药理学杂志,2004,22(3):559 - 561。
Kalaria RN, Premkumar DR, Lin CW, Kroon SN, Bae JY, Sayre LM, LaManna JC:动物脑血管脉络膜组织中Na+/H+交换物的鉴定及其与amilorine敏感[3H]MIA结合的RT-PCR分析。中国生物医学工程学报,1998,31(2):387 - 387。
林德琳,施耐德K, Simmons DM, Baron R, Lee BS, Kopito RR:脉络膜丛阴离子交换器的功能表达和亚细胞定位。美国国家科学促进会。[j] .中国科学:地球科学。
Halmi P, Parkkila S, Honkaniemi J: kainic酸诱导癫痫持续状态大鼠脑内碳酸酐酶II、IV、VII、VIII和XII的表达。神经化学杂志,2006,48:24-30。
马塞金,李建平,李建平,等。大鼠脑脊液中脉络膜蛋白的表达与衰老的关系。中国生物医学工程学报,2005,26(6):917-927。
Mani-Ponset L, Masseguin C, Davet J, Herbute S, Maurel D, Ghandour MS, Reiss-Bubenheim D, Guell A, Gabrion J: 11天太空飞行对发育中的大鼠脉络丛的影响。脑卒中研究与发展,1997,19(3):387 - 398。
Maren TH, Conroy CW, Wynns GC, Godman DR:一种高分子量碳酸酐酶抑beplay靠谱制剂的肾和脑脊液形成药理学。中华药理学杂志,1997,28(3):391 - 391。
张建军,张建军,张建军,等:慢性乙酰唑胺治疗后脉络膜丛上皮表面超微结构的变化。[J] .中华医学杂志,1998,27(2):333-342。
马波,向勇,穆世民,李涛,于明明,李晓军:乙酰唑胺和正二醇对注射AQP1-cRNA的非洲爪蟾卵细胞渗透性的影响。医药学报,2004,25:90-97。
向勇,马波,李涛,高建伟,于海明,李晓军:乙酰唑胺抑制水通道蛋白-1的表达和血管生成。医药学报,2004,25:812-816。
穆思敏,季晓华,马波,于海明,李晓军:乙酰唑胺对大鼠肾近端小管上皮细胞差异蛋白的影响及其与AQP1抑制的关系。姚学学报,2003,38:169-172。
于海明,孙博明,白强,小田世生,李晓军:乙酰唑胺对大鼠睾丸AQP1基因表达及附睾精子数量/活力的影响。科学通报,2002,32(1):1- 4。
文勇,洪书军,申丹,郑勇:系统性低钠血症后脉络膜丛上皮水通道蛋白-1表达的升高。神经科学通报,2006,35(3):1-6。
Masseguin C, Mani-Ponset L, Herbute S, Tixier-Vidal A, Gabrion J:短期头向下倾斜后大鼠脉络膜丛上皮紧密连接的持续性、顶端结构和蛋白表达的变化。中华神经科杂志,2001,30(3):357 - 357。
李建军,李建军,李建军。水通道蛋白1和水通道蛋白4在大鼠脉络膜丛中的表达。生物化学学报,2003,16(9):80-86。
Brown PD, Davies SL, Speake T, Millar ID:脑脊液生成的分子机制。beplay靠谱神经科学学报,2004,29(1):957-970。
王晓明,王晓明,王晓明,等。水通道蛋白-1在脉络膜丛中表达的研究进展。中华神经科学杂志,2006,26(6):711 - 719。
Johansson PA, Dziegielewska KM, Ek CJ, Habgood MD, Mollgard K, Potter A, Schuliga M, Saunders NR:发育中的哺乳动物脑脉络膜丛水通道蛋白-1的表达。中国生物医学工程学报,2005,32(2):353-364。
李建军,李建军,李建军,李建军。水通道蛋白-1和水通道蛋白-4在脑膜发育中的作用。中华神经科杂志,2006,24(4):391 - 391。
李丽娟,李丽娟,李丽娟,等。水通道蛋白CHIP在内皮细胞中的表达。美国国家科学促进会。[j] .中国科学:地球科学。
Lehmann GL, Gradilone SA, Marinelli RA:中枢神经系统水通道蛋白水通道。中华神经科杂志,2004,31(1):393 - 393。
吴强,张建军,张建军,张建军。Na+-K+- 2cl -共转运蛋白在脉络膜丛细胞中的功能研究。中国生物医学工程学报,2009,31(2):559 - 564。
王晓明,王晓明,王晓明,等。脑水通道蛋白的研究进展。神经科学学报,2004,29(4):947-955。
金建刚,孙玉军,尹超,金毅,南宫,朴建辉,Park SK, Ojeda SR, D'Elia AV, Damante G, Lee BJ:甲状腺转录因子-1通过调节脑水通道蛋白-1的合成促进脑脊液形成。beplay靠谱生物化学学报,2007,28(2):14923-14931。
王晓明,王晓明,王晓明,王晓明,王晓明,王晓明。脉络膜丛水通道水通道蛋白-1缺失对小鼠脑脊液生成和颅内压的影响。beplay靠谱刘建军,刘建军,等。
王志强,宋勇,王志强。水通道蛋白-1缺失对脑脊液产生的影响。beplay靠谱中华神经科杂志,2003,26(6):525-528。
Preston JE:老化脉络膜丛-脑脊液系统。beplay靠谱生物工程学报,2001,32(2):531 - 537。
lonatti PL, Basaldella L, Orvieto E, Fiorindi A, Carteri A:脉络膜丛和水通道蛋白-1:脑脊液产生的新解释。beplay靠谱小儿神经外科,2004,40:277-283。
Scavone C, Scanlon C, McKee M, Nathanson JA:心房利钠肽通过环GMP和环GMP依赖性蛋白激酶调节钠钾活化腺苷三磷酸酶的机制。中华药理学杂志,1997,26(2):344 - 344。
Preston JE, McMillan PN, Stopa EG, Nashold JR, Duncan JA, Johanson CE:心房利钠肽诱导脉络膜丛黑色上皮细胞:脑积水脑脊液下调模型的一致性。儿科外科杂志,2003,13(增刊1):40-42。
刘建军,张建军,张建军,张建军。avpv1受体介导的脉络膜丛上皮细胞Cl-外排减少和暗细胞数量增加。中国生物医学工程学报,2009,32(2):559 - 564。
Faraci FM, Mayhan WG, Heistad DD:加压素对脑脊液产生的影响:加压素(V1)受体的可能作用。beplay靠谱[J] .中国生物医学工程学报,2009,25(4):394 - 398。
王海燕,王海燕,王海燕,等。大鼠脉络膜丛钠肽及其受体的表达。第二届国际脉络丛工作坊,2003,国王学院;英国伦敦
Carcenac C, Herbute S, Masseguin C, Mani-Ponset L, Maurel D, Briggs R, Guell A, Gabrion JB:后肢悬吊和航天飞行对大鼠脉膜丛cGMP水平的影响。重力物理学报,1999,6:17-24。
Steardo L, Nathanson JA:脑屏障组织:心房肽的终末器官。科学,1987,35:470-473。
Mori K, Tsutsumi K, Kurihara M, Kawaguchi T, Niwa M:诱导或先天性脑积水大鼠脉络膜丛心房钠肽受体的改变。儿童神经系统,1990,6:190-193。
Herbute S, Oliver J, Davet J, Viso M, Ballard RW, Gharib C, Gabrion J:太空飞行9天后SLS-1大鼠脉络膜丛中ANP结合位点的增加。航空航天与环境医学,1994,(5):134-138。
张建军,张建军,张建军,等。抗利尿激素结合位点在阿尔茨海默病中的表达。中国生物医学工程学报,1996,25(6):559 - 564。
李晓东,李晓东,李晓东,等。阿尔茨海默病患者脑脊液压力升高的临床意义。beplay靠谱beplay靠谱脑脊液杂志,2006,3:7-
Albeck MJ, Skak C, Nielsen PR, Olsen KS, Borgesen SE, Gjerris F:脑脊液流出阻力的年龄依赖性。beplay靠谱中华神经外科杂志,1998,32(3):379 - 379。
barbio - micahely E, Mayevsky A:颅内压升高大鼠模型的多参数监测。中华神经创伤杂志,2001,18:711-725。
Doczi T, Joo F, Vecsernyes M, Bodosi M:动脉瘤性蛛网膜下腔出血患者脑脊液心房利钠因子浓度升高和颅内压升高。beplay靠谱神经外科,1988,23:16-19。
Akdemir G, Luer MS, Dujovny M, Misra M:脑室内房利钠肽治疗急性颅内高压。中华神经科杂志,1997,19(5):515- 521。
Minamikawa J, Kikuchi H, Ishikawa M, Yamamura K, Kanashiro M:心房利钠肽对先天性脑积水大鼠脑水肿、颅内压和脑能代谢的影响。神经科杂志(维也纳)。1994, 60: 104-106。
Johanson CE, Donahue JE, Spangenberger A, Stopa EG, Duncan JA, Sharma HS:心房利钠肽在脉络膜丛-脑脊液系统的颅内压调节中的作用。神经学报,2006,26(6):451-456。
山崎H,杉野M, Ohsawa N:脑脊液中心房利钠肽对颅内压的可能调节。beplay靠谱中华神经科杂志,1997,38(3):88-93。
福岛T:高岭土诱导脑积水犬脑脊液中心房钠肽和环GMP的改变。beplay靠谱《新经济》,1992,44(4):457-462。
张建军,李建军,李建军,等。小儿脑脊液中心钠肽的测定。beplay靠谱儿科学报,1990,30:201-207。
先天性脑积水大鼠脉络膜丛心房利钠肽受体的改变(LEW-HYR和HTX)。《新经济》,1990,42:539-545。
王晓明,王晓明,王晓明,等。二丁基鸟苷-3′-5′环单磷酸对脑脊液流beplay靠谱量的抑制作用。科学进展,1998,37:514-
张建军,张建军,张建军,等。高血压大鼠脉络膜丛中利钠肽A受体的表达和cGMP的产生。中华神经科杂志,1998,33(3):369 - 369。
Hammer M, Sorensen PS, Gjerris F, Larsen K:正常压力脑积水合并良性颅内高压患者脑脊液beplay靠谱中加压素的含量。内分泌学报(哥本哈根)。[j] .中国科学:地球科学。
Jones HC, Deane R, Bucknall RM:大鼠脑脊液压力和吸收阻力的发育变化。beplay靠谱中国生物医学工程学报,2009,31(3):559 - 559。
李建军,李建军,李建军。大鼠脑脉络膜丛水电解质分布的研究。中国生物医学工程学报,2002,31(2):344 - 344。
Pershing LK, Johanson CE:酸中毒诱导的脉络膜丛Na-K交换泵活性增强:脑脊液pH稳态可能作用的个体发生分析。beplay靠谱中华神经科杂志,2002,32(3):332 -332。
张建军,张建军,张建军,等。大鼠脉络膜丛和大脑皮层血流量的变化。[J] .中国生物医学工程学报,2009,32(2):559 - 563。
刘建军,刘建军,刘建军,等。[123I]异丙基多巴安非他命与99mtc -高技术酸盐在脑和脉络膜丛中摄取差异的研究。中国生物医学工程杂志,1997,19(3):379-384。
张建平,张建平。幼鼠脉络膜丛钾转运能力的发育。[J] .生物医学工程学报,2009,25(2):591 - 591。
Johanson CE, Parandoosh Z, Dyas ML:乙酰唑胺改变脉络膜丛、脑脊液和大脑pH和HCO3的成熟差异。beplay靠谱[J] .中国生物医学工程学报,2002,26(2):559 - 564。
Smith QR, Woodbury DM, Johanson CE: [36Cl]-, [22Na]-和[3H]甘露醇摄取到体内脉络膜丛-脑脊液脑系统的动力学分析:血脑和血- csf屏障的发生。beplay靠谱中国生物医学工程学报,2009,25(3):391 - 398。
Johanson C, Woodbury D:发育大鼠脑脊液流量和细胞外空间的变化。药物和发育中的大脑。编辑:Vernadakis A, Weiner N. 1974,纽约:全会出版社,281-287。
Bering EA:脑脊液的循环。beplay靠谱脉络膜丛作为液体流动和心室扩大力的产生器的演示。中华神经外科杂志,1999,19(4):559 - 561。
Jones HC, Bucknall RM: H-Tx大鼠先天性脑积beplay靠谱水发展期间脑脊液压力和侧脑室流出量的变化。中国生物医学工程学报,1997,28(3):573-583。
Jones HC, Lopman BA:脑积水HTx大鼠脑脊液压力与心室扩张的关系。小儿外科杂志,1998,8(增刊1):55-58。
Kaiser G, Jones HC:先beplay靠谱天性脑积水10日龄大鼠的脑脊液压力。小儿外科杂志,1991,1(增刊1):20-22。
Owen-Lynch PJ, Draper CE, Mashayekhi F, Bannister CM, Miyan JA:脑积水大鼠皮层发育异常的细胞周期控制缺陷。中国生物医学工程学报,2003,26(6):623-631。
Miyan JA, nabiyoui M, Zendah M:脑发育:脑脊液的重要作用。beplay靠谱中国生物医学工程杂志,2003,31(1):317-328。
david BE, Robinson ML: hy3小鼠的先天性脑积水是由Hydin(一种大型新基因)的移码突变引起的。中国生物医学工程学报,2003,12(2):563 - 567。
Banizs B, Pike MM, Millican CL, Ferguson WB, Komlosi P, Sheetz J, Bell PD, Schwiebert EM, Yoder BK:纤毛功能障碍导致室管膜和脉络丛功能改变,并导致脑积水的形成。发展,2005,32(2):5329-5339。
马夏叶,王志强,张志强。神经生长因子在先天性脑积水患儿脑脊液中的表达。beplay靠谱中国生物医学工程学报,2009,31(2):632-637。
Nadvi SS, Annamalai K, Naicker VL, Govender UG, Nathoo N, Van Dellen JR, Bhigjee AI: 5例先天性脑积水患者细胞因子表达的初步报告。中华医学杂志,1999,26(6):696-699。
Del Bigio MR:脑积水引起的脑脊液成分改变。beplay靠谱神经外科。1989,25:416-423。
Hayamizu TF, Chan PT, Johanson CE:成年大鼠室管膜和脉络膜丛中FGF-2的免疫反应:对全脑缺血和脑室内FGF-2的反应。中华神经科杂志,2001,23:353-358。
Johanson CE, Palm DE, Primiano MJ, McMillan PN, Chan P, Knuckey NW, Stopa EG:短暂性前脑缺血后脉膜丛恢复:生长因子的作用及其他修复机制。中国生物医学工程学报,2009,29(2):559 - 561。
Martinez-Pena y Valenzuela I, Carmona-Calero EM, Perez-Gonzalez H, Ormazabal-Ramos C, Fernandez-Rodriguez P, Gonzalez-Marrero I, Castaneyra-Perdomo A, Ferres-Torres R:动脉高血压和心室扩张中脑脊液蛋白和合下器beplay靠谱官分泌的变化。SHR大鼠的研究。中华病理学杂志,2006,21:179-185。
Somera KC, Jones HC:在H-Tx大鼠脑积水中,输水管关闭和脑室扩张之前,联合下器官糖蛋白免疫反应性降低。中国生物医学工程学报,2004,31(3):361-373。
交合下器官的室管膜分泌细胞:在脑积水中起什么作用?中国生物医学工程学报,2007,29(3):463-468。
Perez-Figares JM, Jimenez AJ, Rodriguez EM:关节下器官,脑脊液循环和脑积水。beplay靠谱中国生物医学工程学报,2001,28(2):591- 597。
Socci DJ, Bjugstad KB, Jones HC, Pattisapu JV, Arendash GW:氧化应激与H-Tx大鼠模型中遗传性脑积水病理生理相关的证据。中国生物医学工程学报,2004,25(5):559 - 561。
Kawamata T, Katayama Y, Tsuji N, Nishimoto H:大鼠脑积水海马CA3区域的选择性易感性与保留血流的间质性脑水肿代谢紊乱。中华神经科杂志,2003,26(6):545-547。
Klinge PM, Samii A, Muhlendyck A, Visnyei K, Meyer GJ, Walter GF, Silverberg GD, Brinker T:成人高岭土脑积水诱导后脑灌注不足和海马反应延迟。中风。2003,34:193-199。
Del Bigio MR, Bruni JE, Vriend JP:脑积水诱导后成熟兔脑内单胺类神经递质及其代谢物。中华神经医学杂志,1998,23(3):1379-1386。
Balasubramaniam J, Del Bigio MR:脑积水诱导大鼠脑基因表达谱的年龄依赖性改变分析。中国生物医学工程学报,2002,17(3):559 - 561。
McAllister JP, Chovan P:新生儿脑积水。机制和后果。中华神经外科杂志,1998,9:73-93。
Del Bigio MR, Bruni JE:硅油致兔脑积水。儿童神经系统,1997,7:79-84。
Raisis JE, Kindt GW, McGillicuddy JE, Miller CA:脑beplay靠谱积水患者的脑脊液乳酸和乳酸/丙酮酸比值。中华神经外科杂志,1997,44(4):337-341。
Schalk KA, Faraci FM, Williams JL, VanOrden D, Heistad DD:心房肽对脑脊液生成的影响。beplay靠谱[J]中华血液学杂志,1997,12(2):691-696。
张志强,张志强,张志强,等。血管紧张素和心房利钠肽对脑循环的影响。[J]中华血液学杂志,1997,12(3):318- 326。
Tsugane S, Suzuki Y, Kano T, Takayasu M, Shibuya M, Sugita K:血管内和动脉内给药后血管加压素对犬局部脑血流的影响。生命科学,1994,54:PL241-246。
张建军,张建军,张建军,张建军,张建军。高血压大鼠蛛网膜下腔出血后心房钠肽分泌的研究进展。中国生物医学工程学报,1997,17(4):641-648。
Naruse S, Aoki Y, Horikawa Y, Tanaka C, Higuchi T, Ebisu T, Ueda S, Kondo S, Kiyota T, Hayashi H:质子磁共振法评价心房利钠肽对缺血性脑水肿的影响。神经科杂志(维也纳)。1990, 51(1): 248-250。
Codman和Camino颅内压传感器同步连续颅内压(ICP)信号的比较。医学工程物理,2006,28:542-549。
Brean A, Eide PK, Stubhaug A:脑实质和脑室内同时测量的颅内压的比较。临床监测计算[J] . 2006,20: 411-414。
Czosnyka Z, Czosnyka M, Pickard JD:脑脊液脉压和B波。中华神经外科杂志,2005,30(3):767-768。作者回复768。
Momjian S, Czosnyka Z, Czosnyka M, Pickard JD:常压脑积水颅内血管源性波与脑脊液流出阻力的关系。beplay靠谱中华神经外科杂志,2004,18:56-61。
张建军,张建军,张建军,张建军。脑脊液动力学。beplay靠谱物理学报,2004,25(1):51-76。
张志强,张志强,张志强。脑积水分流术与颅内压波的关系。医学与工程计算,2005,43(3):71-77。
Codman和Camino颅内压传感器同步连续颅内压(ICP)信号的比较。医学工程物理,2008,30:34-40。
Eide PK:一种处理连续颅内压信号的新方法。医学工程物理,2006,28:579-587。
Eide PK:使用一种处理颅内压信号的新方法评估儿童颅内压记录。小儿神经外科,2005,41:122-130。
儿童连续颅内压记录的质量评估。小儿神经外科,2006,42:28-34。
Eide PK:脑室-腹膜分流治疗特发性常压脑积水患者的颅内压参数。神经学报(维也纳)。[j] .中国科学:地球科学。29日的讨论。
Eide PK, Sorteberg W:特发性常压脑积水患者分流治疗1年后术前脊柱流体动力学与临床变化。中华神经外科杂志,2005,19:475-483。
Eide PK, Brean A:在术前评估可能患有特发性常压脑积水的受试者时确定颅脉压振幅水平。神经学报(维也纳)。[j] .中国科学:地球科学。讨论1156年。
Foss T, Eide PK, Finset A:分流治疗后认知功能改善或不改善的特发性常压脑积水患者的颅内压参数。老年精神疾病,2007,23:47-54。
Stephensen H, Andersson N, Eklund A, Malm J, Tisell M, Wikkelso C:目的分析55例非交通性和交通性脑积水的B波特征。中华神经外科杂志,2005,26(6):965-970。
Lenfeldt N, Andersson N, Agren-Wilsson A, Bergenheim AT, Koskinen LO, Eklund A, Malm J:脑beplay靠谱脊液脉压法检测脑B波的可能替代方法。中华神经外科杂志,2004,31(1):944- 951。
Querfurth HW, Arms SW, Lichy CM, Irwin WT, Steiner T:无创经眼静脉和动脉血流动力学测量预测颅内压:一项初步研究。中华神经科杂志,2004,(1):183-194。
Heese O, Regelsberger J, Kehler U, Westphal M:中空mandrin在心室外引流中的应用。神经学报(维也纳)。[j] .中国科学:地球科学。
Czepko R, Cieslicki K, Niedzwiedzki J, Libionka W, Pietraszko W:克拉科夫贾盖隆大学神经外科连续颅内压和脑灌注压监测系统的数据采集、记录和处理可能性。李志强,2005,32(2):1- 4。
张建军,张建军,张建军,张建军,张建军,张建军。脑电图在脑积水诊断中的应用。中华神经创伤杂志,2002,22:836-843。
Linninger AA, Tsakiris C, Zhu DC, Xenos M, Roycewicz P, Danziger Z, Penn R:人脑脉动脑脊液动力学。beplay靠谱生物医学工程学报,2005,32(2):557-565。
Pena A, Harris NG, Bolton MD, Czosnyka M, Pickard JD:通讯性脑积水:进行性脑室扩大的生物力学再探讨。神经学报,2002,31(1):59-63。
Pena A, Bolton MD, Whitehouse H, Pickard JD:脑室形状对脑室周围生物力学的影响:有限元分析。神经外科杂志,1999,45:107-116。讨论116 - 108。
Ghersi-Egea JF, Finnegan W, Chen JL, Fenstermacher JD:经蛛网膜下腔静脉滴注蔗糖进入大鼠脑脊液池的快速分布。beplay靠谱神经科学学报,1996,25(5):1271-1288。
Nagaraja TN, Patel P, Gorski M, Gorevic PD, Patlak CS, Fenstermacher JD:在正常大鼠中,脑室内注射胰岛素样生长因子-1从脑脊液中迅速清除,进入大脑的分布有限。beplay靠谱脑脊液杂志,2005,2:5-
王晓明,王晓明,王晓明,等。脑脊液对脑水肿的清除作用。beplay靠谱血管源性脑水肿的解决机制。中华神经外科杂志,1997,28(4):754-764。
Pickard JD, Coleman MR, Czosnyka M:脑积水、脑室肿大和植物人状态:综述。中华心理医学杂志,2005,25(5):344 - 344。
Marmarou A, Bergsneider M, Klinge P, Relkin N, Black PM:特发性常压脑积水术前评估补充预后试验的价值。神经外科杂志,2005,57:517 - 528。ii-v讨论。
Shapiro K, Marmarou A, Shulman K:临床脑脊液动力学和神经轴顺应性的表征使用压力-容积指数:1 .正常压力-容积指数。中国生物医学工程学报,1997,7(5):559 - 561。
Chahlavi A, El-Babaa SK, Luciano MG:成人发病脑积水。中华神经外科杂志,2001,12:753-760。
姚洋,姚洋,罗克奇,梅奥M, Silverberg GD, McGuire D:脑脊液引流术对阿尔茨海默病患者脑脂质过氧化的影响。中华老年痴呆症杂志,2004,6:385-389。
Pourghasem M, Mashayekhi F, Bannister CM, Miyan J:早发性脑积水大鼠胎儿脑脊液通路的变化。小儿外科杂志,2001,11(增刊1):10-13。
Nojima Y, Enzan H, Hayashi Y, Nakayama H, Kiyoku H, Hiroi M, Mori K:先天性脑积水HTX大鼠神经上皮和室管膜改变的超微结构和免疫组织化学研究。中华病毒学杂志,1998,48(1):115-125。
Nilsson C, Stahlberg F, Thomsen C, Henriksen O, Herning M, Owman C:磁共振成像测量人类脑脊液生产的昼夜变化。beplay靠谱[J] .中国生物医学工程学报,2002,26(2):559 - 564。
Johanson CE, Szmydynger-Chodobska J, Chodobski A, Baird A, McMillan P, Stopa EG: fgf -2诱导的脑积水形成和体积吸收的改变。beplay靠谱中国生物医学工程学报,2009,27(3):563 - 567。
黄春华,黄春华,黄春华,等。生长因子对离体脉络膜丛脑脊液形成的调节作用:FGF-2与tgf - β 1。小儿外科杂志,2000,10(增刊1):44-46。
Knuckey NW, Preston J, Palm D, Epstein MH, Johanson C:脑积水减少脉络膜丛上皮氯离子外排。中国生物医学工程学报,2003,18(3):313-317。
Ridgway JP, Turnbull LW, Smith MA:使用磁共振相位成像的脉冲脑脊液流动演示。中华放射医学杂志,1997,26(3):423-427。
Maeder P, Gudinchet F, Meuli R, Fankhauser H:内镜下经皮脑室造瘘术中脑脊液流动beplay靠谱的动态MRI。中华神经外科杂志,1998,12:18-22。
Nilsson C, Stahlberg F, Gideon P, Thomsen C, Henriksen O: β 1受体拮抗剂可抑制人脑脊液夜间分泌的增加。beplay靠谱中国生物医学工程学报,2009,32(4):444 - 444。
陈建军,陈建军,陈建军,陈建军,陈建军,陈建军,陈建军,陈建军。beplay靠谱[J]中华血液学杂志,2007,27(4):563- 572。
McCormack EJ, Egnor MR, Wagshul ME:使用相对比平衡稳态自beplay靠谱由进动改进脑脊液流量测量。医学影像,2007,25(2):172-182。
Knuckey NW, Finch P, Palm DE, Primiano MJ, Johanson CE, Flanders KC, Thompson NL:短暂性前脑缺血后大鼠海马转化生长因子β亚型的差异表达。中国生物医学工程学报,1996,25(4):391 - 391。
张建军,张建军,张建军,张建军,等。前脑缺血后脉络膜丛电解质的超微结构研究。中国生物医学工程学报,2009,32(4):557 - 557。
Fernandez-Carriera RA, Gonzalez-Quevedo A, Lara-Rodriguez RF, Leon-Ortiz MM, Gonzalez-Garcia S, Vicente-Valdes I:缺血性脑血管病患者脑脊液蛋白的电泳。beplay靠谱中华神经科杂志,2002,35(5):998 - 998。
Sharma HS, Duncan JA, Johanson CE:大鼠全身热疗破坏血脑脊液屏障,诱发脑水肿。beplay靠谱神经学报,2006,26(6):426-431。
Drake J:心室裂裂综合征。中华神经外科杂志,2005,32(2):557 - 558。讨论258 - 259。
王晓明,王晓明,王晓明,等。脑脊液系统顺应性和流出阻力的区室分析。beplay靠谱中华神经外科杂志,1997,18(3):523-534。
郑丽丽,李建军,李建军,李建军,李建军。基于神经网络的脑积水脉搏模型研究。小儿神经外科杂志,2002,36:281-303。
Jacobs S, Ruusuvuori E, Sipila ST, Haapanen A, Damkier HH, Kurth I, Hentschke M, Schweizer M, Rudhard Y, Laatikainen M, Tyynela J, Praetorius J Voipio J, Hubner CA: Slc4a10基因靶向破坏小鼠脑室小,神经元兴奋性降低。美国国家科学促进会。[j] .中国科学:地球科学,2008。
Milhorat TH, Hammock MK, Davis DA, Fenstermacher JD:脉络膜丛乳头状瘤。1 .脑脊液生产过剩的证beplay靠谱据。儿童脑科学,1997,22(2):273-289。
guevas P, Gimenez-Gallego G:成纤维细胞生长因子与脑积水。中华神经科杂志,2002,22(2):102-104。
Al-Sarraf H, Philip L:高血压对大鼠血脑完整性和血CSF屏障、脑血流和CSF分泌的影响。中国生物医学工程学报,2003,25(3):379 - 388。
王晓明,王晓明,王晓明,等。高血压大鼠脉络膜丛的超微结构研究。[J] .中国生物医学工程学报,1994,5(5):851-856。
王晓明,王晓明,王晓明,等。原发性高血压大鼠血管脉络丛和红细胞[Na+, K+, Cl-]-共转运系统的研究。高血压的细胞方面。编辑:Bruschi G, Borghetti A. 1992,柏林-海德堡-纽约:Springer-Verlag, 257-261。
Murphy VA, Johanson CE:肾上腺素能诱导的脑屏障系统对小非电解质的渗透性增强:脉络膜丛与脑毛细血管。[J]中华血液学杂志,1997,25(5):391 - 391。
刘建军,张建军,张建军,等。成纤维细胞生长因子与血脑屏障的关系。生物活性肽手册。编辑:Kastin A, Pan W. 2006,阿姆斯特丹:爱思唯尔,1467-1472。
大脑组织的体积调节——一项调查。神经学报(维也纳)。1993, 21(1): 1-8。
杨建军,杨建军,杨建军,等。抗利尿激素对小鼠室管膜和毛细血管对微量水渗透性的影响。[J] .中国生物医学工程学报,2006,31(1):489 -489。
Rodriguez EM:脑脊液作为beplay靠谱神经内分泌整合的途径。中华内分泌杂志,2002,31(1):444 - 444。
Rodriguez EM, Heller H:蟾蜍脉络膜丛的抗利尿活性和超微结构。[J]中华内分泌杂志,1997,26(4):391 - 391。
Schultz WJ, Brownfield MS, Kozlowski GP:下丘脑-脉络膜束。2脉络膜丛对血管加压素的超微结构反应。中国生物医学工程学报,1997,18(3):559 - 561。
Brownfield MS, Kozlowski GP:下丘脑-脉络膜束。1 .脑端脉络膜丛和脑脊液神经素通路的免疫组织化学证明。beplay靠谱中国生物医学工程学报,1997,18(3):391 - 391。
李建军,李建军,李建军,李建军,李建军,李建军,李建军,李建军。精氨酸加压素在大鼠脉络膜丛上皮组织中的表达及表达。脑卒中与脑卒中杂志,1997,28(4):663 - 668。
黄春华,黄春华,黄春华,等。FGF-2在脉络膜丛和脑垂体中的表达。儿科外科杂志,2001,11(增刊1):37-38。
陈毅,陈毅,张晓明,等。avp介导的非神经元性脑细胞在细胞、器官和全身水平上对水空间的调节。中华神经科学杂志,2000,32(2):449 - 449。
陈志刚,陈志刚,陈志刚,陈志刚。成纤维细胞生长因子受体与血管加压素在脉络膜丛上皮细胞中的分布及共定位。中华神经医学杂志,2002,13:257-259。
Zemo DA, McCabe JT:盐负荷增加下丘脑和脉络膜丛血管加压素和血管加压素1b受体mRNA。中华神经科杂志,2001,35(5):391 - 398。
李春华,李春华,李春华,等。利钠肽在心脏保护中的作用。中华心血管病杂志,2006,29(4):368 - 368。
Saavedra JM, Kurihara M:心房钠素受体在大鼠脑中的放射自显影。[J]中国生物医学工程学报,2001,29(3):557 - 557。
王晓明,王晓明,王晓明,等。心房利钠肽受体在高血压大鼠脑微血管和脉络膜丛中的表达。中国生物医学工程学报,2009,35(2):391 - 391。
张建军,张建军,张建军,等。高血压大鼠心房钠肽与脑钠肽的结合。中国生物医学工程学报,2009,31(2):393 - 398。
高血压和脱水时大鼠脑核心房钠肽受体的变化。中国生物医学工程学报,1998,25(3):387 - 398。
乔杜斯基A, Szmydynger-Chodobska J, Johanson CE:加压素介导中枢血管紧张素II对脑脊液形成的抑制作用。beplay靠谱中华药理学杂志,1998,32(4):559 - 561。
Rapoport SI, Schapiro MB, May C:人类衰老过程中高香草酸向脑脊液输送的减少。beplay靠谱中华神经医学杂志,2004,31(1):521 - 524。
王晓明,王晓明,王晓明,等。高岭土诱导的老年脑积水大鼠脑内淀粉样蛋白的积累。神经病学杂志,2006,17:657-660。
胡士德,李志强,李志强。猫脉络膜丛对脑脊液碳酸氢盐的调节。beplay靠谱中国生物医学工程学报,2009,32(2):444 - 444。
胡士德,李志强,李志强。猫脉络膜丛对脑脊液钾的调控。beplay靠谱中国生物医学工程学报,2006,32(2):557 - 557。
李建平,李建平,李建平,等。微量营养素在脉络膜丛和肾脏中的转运:药物治疗的意义。医药杂志,2006,23:2515-2524。
刘建军,刘建军,刘建军,等。脑脊液在阿尔茨海默病中的表达和转运。血-脑脊液屏障beplay靠谱编辑:郑伟,Chodobski A. 2004, Boca Raton: CRC Press LLC, 307-339。
Zipser BD, Johanson CE, Gonzalez L, Berzin TM, Tavares R, Hulette CM, Vitek MP, Hovanesian V, Stopa EG:阿尔茨海默病的微血管损伤和血脑屏障渗漏。中华神经医学杂志,2007,28:977-986。
Donahue JE, Flaherty SL, Johanson CE, Duncan JA, Silverberg GD, Miller MC, Tavares R,杨伟,吴强,Sabo E,等:RAGE, LRP-1与阿尔茨海默病淀粉样蛋白- β的关系。中华神经科杂志,2006,31(2):457 - 457。
李建军,李建军,李建军,李建军,李建军,李建军,李建军,李建军,李建军,李建军,李建军,李建军。beplay靠谱中华神经医学杂志,2002,13:611-615。
冯志刚,王志刚,王志刚,王志刚,王志刚:脑脊髓液中疾病标志物的脂质组学分析。beplay靠谱疾病杂志,2006,22:39-64。
Serot JM, Bene MC, Faure GC:脉络膜丛、脑老化与阿尔茨海默病。生物科学前缘,2003,8:515-521。
李建军,张建军,张建军,张建军,张建军,张建军,张建军,张建军,张建军,张建军,张建军,张建军,张建军。低密度脂蛋白受体相关蛋白-1在血脑屏障中对阿尔茨海默病淀粉样蛋白- 1-40肽的清除作用。[J]中国临床医学杂志,2002,26(3):369 - 369。
Muldoon LL, Soussain C, Jahnke K, Johanson C, Siegal T, Smith QR, Hall WA, Hynynen K, Senter PD, Peereboom DM, Neuwelt EA:中枢神经系统恶性肿瘤的化疗递送问题:现实检查。中华临床医学杂志,2007,25(5):595 - 595。
李建军,张建军,李建军,等。脑脊髓液糖化蛋白与老年痴呆症的关系。beplay靠谱中国生物医学工程学报,2001,22(2):397-402。
Spector R, Johanson CE:大脑中脱氧核苷的起源:对神经发生和干细胞治疗研究的意义。医药杂志,2007,24:859-867。
哺乳动物中枢神经系统的核苷和维生素稳态。杨建军,刘志强,等。中国农业科学学报,2004,26(1):344 - 344。
杨建军,李建军,李建军,等。脱氧核苷和维生素在中枢神经系统中的转运。美联储学报,1984,43:196-200。
Dickson PW, aldrred AR, Marley PD, Bannister D, Schreiber G:大鼠脉络膜丛负责甲状腺转甲状腺素(前白蛋白)的合成和分泌。脉络膜丛的转甲状腺素合成调节独立于肝脏。中国生物医学工程学报,2006,31(2):379 - 379。
张建军,张建军,张建军,张建军。甲状腺素与阿尔茨海默病的相关性研究。中国生物医学工程学报,2007,28(2):713-718。
陈瑞林,Athauda SB, Kassem NA,张勇,Segal MB, Preston JE:老龄羊血脑脊液屏障促甲状腺素合成的降低。beplay靠谱[J]中国生物医学工程学报,2002,26(3):559 - 558。
陈建军,陈建军,陈建军,等。脑脊髓液甲状腺素转运与老年痴呆症的关系。beplay靠谱中华神经外科杂志,1997,26(3):563 - 568。
Li MD, Kane JK, Matta SG, Blaner WS, Sharp BM:尼古丁增强大鼠脉络膜丛转甲状腺素的生物合成和分泌:对β -淀粉样蛋白形成的影响。中华神经科学杂志,2000,20(2):318- 323。
Stopa EG, Berzin TM, Kim S, Song P, Kuo-LeBlanc V, Rodriguez-Wolf M, Baird A, Johanson CE:人脉络膜丛生长因子对阿尔茨海默病脑脊液动力学的影响。中国生物医学工程学报,2001,32(4):444 - 444。
Anthony SG, Schipper HM, Tavares R, Hovanesian V, Cortez SC, Stopa EG, Johanson CE:应激蛋白在阿尔茨海默病脉络膜丛中的表达。中华老年痴呆症杂志,2003,5:171-177。
Dietrich MO, Spuch C, Antequera D, Rodal I, de Yebenes JG, Molina JA, Bermejo F, Carro E: Megalin介导瘦素在血- csf屏障中的转运。《神经生物学与衰老》2007
Crossgrove JS,李广军,郑伟:脉络膜丛清除脑脊液中的β -淀粉样蛋白。beplay靠谱Exp生物医学(Maywood)。[j] .中国科学:地球科学。
文克塔克瑞斯南,陈志强,陈志强,陈志强,陈志强,陈志强,陈志强,陈志强,陈志强。脑脊髓液暴露对Mdr1 p -糖蛋白底物CP-615,003中枢神经系统药代动力学的影响。beplay靠谱中国医药杂志,2007,35(5):1341-1349。
庄士敦M, Boulton M, Flessner M:脑脊液吸收的再beplay靠谱研究:颅外淋巴管是否起作用?神经学家。2000,6:77-87。
王晓明,王晓明,王晓明,等。脉络膜丛-脑脊液系统的神经内分泌调节机制。beplay靠谱脑电研究,1997,17(1):109-138。
Tisell M, Tullberg M, Mansson JE, Fredman P, Blennow K, Wikkelso C:脑脊液动力学差异不影响导水管狭窄beplay靠谱和特发常压脑积水患者脑脊液生化标志物水平。中华神经医学杂志,2004,11:17-23。
Tullberg M, Mansson JE, Fredman P, Lekman A, Blennow K, Ekman R, Rosengren LE, Tisell M, Wikkelso C:脑脊液硫脂含量对常压脑积水和皮质下动脉硬化性脑病的影响。中华神经外科杂志,2002,26(3):391 - 391。
张建军,张建军,张建军,等。维生素B在哺乳动物脑内代谢中的应用研究进展[J] .生物医学工程学报,2007,29(3):559 - 559。
张建平,张建平,张建平,等。大鼠脑内放射性标记聚乙二醇和白蛋白的外排。[J] .中国生物医学工程学报,2001,24(2):344 - 344。
Szentistvanyi I, Patlak CS, Ellis RA, Cserr HF:大鼠脑不同区域间质液的引流。中国生物医学工程学报,2004,25(4):557 - 557。
M:《血脑屏障的概念》,1979,奇彻斯特:威利父子有限公司
Rennels ML, Gregory TF, Blaumanis OR, Fujimoto K, Grady PA:哺乳动物中枢神经系统“血管旁”液体循环的证据,由蛛网膜下腔在整个大脑中快速分布的示踪蛋白提供。中国生物医学工程学报,2004,26(3):444 - 444。
Rennels ML, Blaumanis OR, Grady PA:通过血管旁液体途径的快速溶质转运。中华神经科杂志,1990,32(2):431-439。
Proescholdt MG, Hutto B, Brady LS, Herkenham M:侧脑室和大脑池注射示踪剂beplay靠谱[14C]菊粉对大鼠脑脊液流动和渗透的影响。神经科学学报,2000,35(5):577-592。
陈志强,陈志强。有机阴离子转运蛋白在慢性肾功能衰竭进展中的作用。光学学报,2007,11(增刊1):27-31。
刘建军,刘建军,刘建军,等。大鼠脑脊液动力学、脑室扩张和β -淀粉样蛋白保留的研究进展。beplay靠谱脑脊液杂志,2005,2(增刊1):S6-
Stopa EG, Butala P, Salloway S, Johanson CE, Gonzalez L, Tavares R, Hovanesian V, Hulette CM, Vitek MP, Cohen RA:大脑皮质小动脉血管病变、血管β -淀粉样蛋白、平滑肌肌动蛋白、Braak分期和APOE基因型。中风。2008,39:814-821。
李建军,李建军,李建军,李建军,李建军。脑脊液流出阻力评估。beplay靠谱医学与工程学报,2007,45(5):719-735。
Jones HC, Gratton JA:脑积水大鼠脑脊液引流。beplay靠谱幼儿教育,1989,44(增刊1):14-15。
Boon AJ, Tans JT, Delwel EJ, Egeler-Peerdeman SM, Hanlo PW, Wurzer JA, Avezaat CJ, de Jong DA, Gooskens RH, Hermans J:脑脊液流出阻力对正常压力脑积水患者分流反应的预测。中华神经科杂志,1998,31(1):331-333。
Jones HC, Gratton JA:脑脊液压力对幼鼠硬脑膜静脉压力beplay靠谱的影响。中华神经外科杂志,1989,31(1):119-123。
Erlich SS, McComb JG, Hyman S, Weiss MH:兔脑脊液引流嗅觉通路的超微结构形态学。beplay靠谱中华神经外科杂志,2004,26(4):464 -473。
Erlich SS, McComb JG, Hyman S, Weiss MH:兔脑脊液引流眼眶通路的超微结构。beplay靠谱中华神经外科杂志,1997,26(3):526 - 531。
张建军,张建军,张建军,张建军。猪和大鼠脑脊液吸收部位的发育:嗅鼻甲蛛网膜下腔和淋巴管的连接。beplay靠谱Anat Embryol (Berl)。[j] .中国科学:地球科学。
Johnston M, Zakharov A, Papaiconomou C, Salmasi G, Armstrong D:人类、非人类灵长类动物和其他哺乳动物脑脊液与鼻淋巴管之间联系的证据beplay靠谱。beplay靠谱脑脊液杂志,2004,1:2-
张建军,张建军,张建军,张建军,张建军。脑外淋巴管和颅内静脉对绵羊脑脊液吸收的影响。beplay靠谱中国生物医学工程学报,2004,32(4):391 - 391。
张建军,张建军,张建军,张建军。脑外淋巴管和蛛网膜绒毛对脑脊液示踪剂清除的影响。中国生物医学工程学报,2009,32(1):444 - 444。
Johnston M, Zakharov A, Koh L, Armstrong D:蛛网膜下注射Microfil揭示非人灵长类动物脑脊液与鼻淋巴的联系。beplay靠谱中华神经科杂志,2005,31(3):632- 664。
Mollanji R, bozanoovic - sosic R, Silver I, Li B, Kim C, Midha R, Johnston M:颅外淋巴通路阻断对颅内压调节的影响。[J] .中国生物医学工程学报,2011,28(2):559 - 561。
Mollanji R, Bozanovic-Sosic R, Zakharov A, Makarian L, Johnston MG:通过筛状板阻断脑脊液beplay靠谱吸收增加静息颅内压。[J] .中国生物医学工程学报,2009,32(2):559 - 563。
刘建军,刘建军,刘建军,等。绵羊脑脊液转运的研究进展。beplay靠谱[J] .中国生物医学工程学报,2011,28(1):555 - 557。
刘建军,刘建军,刘建军,等。脑脊髓液吸收淋巴通路的动力学特性。beplay靠谱中华神经科杂志,1997,14(4):493-498。
张建军,张建军,张建军,等。新生儿脑脊液的吸收是通过蛛网膜突出还是颅外淋巴管发生的。beplay靠谱[J] .中国生物医学工程学报,2009,32(2):559 - 563。
吕德曼,王晓明,王晓明,等:脑脊液沿视神经向淋巴系统流出的超微结构。beplay靠谱儿童神经系统,2005,21:96-103。
Grzybowski DM, Holman DW, Katz SE, Lubow M:脑脊液经人蛛网膜颗粒流出体外模型。beplay靠谱中国眼科杂志,2006,37(4):664- 672。
霍尔曼DW, Grzybowski DM, Mehta BC, Katz SE, Lubow M:人蛛网膜肉芽组织培养细胞骨架和连接蛋白的表达。beplay靠谱脑脊液杂志,2005,2:9-
刘建军,刘建军,刘建军,等。脊髓脊液吸收的研究进展。[J] .中国生物医学工程学报,2009,32(1):444 - 444。
Luedemann W, Kondziella D, Tienken K, Klinge P, Brinker T, Berens von Rautenfeld D:脊髓脑脊液通路及beplay靠谱其在高岭土-脑积水代偿中的意义。神经学报,2002,31(1):271-273。
王晓明,王晓明,王晓明,等。高岭土诱导脑积水患者脑脊液流出通道的铁蛋白示踪研究。中华神经科杂志,2007,33(3):569-575。
沈小强,宫岛,王志刚,等。水通道蛋白- 4在脑积水中的表达及其在脑积水中的代偿作用。中华神经外科杂志,2006,35(5):459-464。
Bloch O, Auguste KI, Manley GT, Verkman AS:高岭土诱导的水通道蛋白-4缺陷小鼠脑积水的加速进展。[J]中华血液学杂志,2006,26(4):557 - 557。
中华神经科学杂志,2006,23:2929-2936。
Johanson CE:脉络膜丛-蛛网膜-脑脊液系统。beplay靠谱神经方法:神经元微环境-电解质和水空间。编辑:Boulton A, Baker G, Walz W. 1988,克利夫顿,新泽西:Humana出版社,9:33-104。
Allen DD, Yokel RA:体内微透析证明不同铝和镓的血脑屏障渗透。中华神经科杂志,2002,28(3):391 - 391。
Knuckey NW, Fowler AG, Johanson CE, Nashold JR, Epstein MH:大池微透析对22Na离子转运和脑脊液动力学的评价。beplay靠谱中华神经外科杂志,1997,24(4):965-971。
Naish JH, Baldwin RC, Patankar T, Jeffries S, Burns AS, Taylor CJ, Waterton JC, Jackson A:治疗抵抗性老年抑郁症脑脊液血流模式异常:微血管病变的潜在生物标志物。中华实用医学杂志,2006,35(6):559 - 561。
Johanson C, Duncan J, Baird A, Stopa E, McMillan P:脉络膜丛在神经保护和神经再生中的重要作用。神经保护与再生,2005,1:77-85。
Ludvig N, Sheffield LG, Tang HM, Baptiste SL, Devinsky O, Kuzniecky RI:大鼠脑膜下药物扩散的组织学证据。中国生物医学工程学报,2008,31(2):344 - 344。
李建军,李建军,李建军,等。钠转运蛋白和水通道蛋白-1在人脉络膜丛中的分布。[J] .中国生物医学工程学报,2006,29(1):559 - 567。
Rao VV, Dahlheimer JL, Bardgett ME, Snyder AZ, Finch RA, Sartorelli AC, Piwnica-Worms D:脉膜丛上皮mdr1p糖蛋白和多药耐药相关蛋白的表达与血脑脊髓液药物通透性屏障的关系。美国国家科学促进会。[j] .中国科学:地球科学。
王晓东,王晓东,王晓东,等。水通道蛋白在脉络膜丛中的生理作用。中国生物医学工程学报,2005,32(1):591 - 596。
致谢
感谢布朗医学院神经外科部门对研究的支持,寿命/罗德岛医院、桑德斯基金会、阿尔茨海默病协会、里希特基金会和美国国立卫生研究院授予NS RO1 27601和NIA RO1 AG027910。我们还要感谢P. McMillan的电子显微镜;N.和J. Johanson负责手稿编辑和绘图;A. Messier和S. Slone的技术贡献;和J. Donahue讨论阿尔茨海默病。
作者信息
作者及单位
相应的作者
额外的信息
相互竞争的利益
作者宣称他们没有竞争利益。
作者的贡献
CEJ主要负责组织和撰写稿件。JAD协助开发儿科和成人脑积水临床方面的材料。PMK和TB对脑脊液压力、高岭土脑积水和脑脊液重吸收有重要意义。EGS有助于解释阿尔茨海默病的病理生理发现。GDS为人类和动物血脑屏障转运蛋白表达和脑脊液在衰老、NPH和痴呆中的动态变化提供了见解;在编辑工作中扮演了重要角色。所有作者都阅读并批准了最终稿件。
作者提交的原始图片文件
下面是作者提交的原始图片文件的链接。
权利和权限
本文由BioMed Central Ltd.授权发表。这是一篇基于知识共享署名许可(http://creativecommons.org/licenses/by/2.0),允许在任何媒体上不受限制地使用、分发和复制,前提是正确引用原创作品。
关于本文
引用本文
约翰逊,c.e.,邓肯,j.a.,克林格,下午et al。脑脊液功能的多样性:健康和疾病的beplay靠谱新挑战。流体屏障5, 10(2008)。https://doi.org/10.1186/1743-8454-5-10
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/1743-8454-5-10
关键字
- 脑积水
- 心房利钠肽
- 脉络丛
- 正常压力脑积水
- 先天性脑积水